题目内容
在密闭容器中的一定量混合气体发生反应:xA(g)+yB(g)?zC(g),平衡时测得:c(A)为0.5mol/L,保持温度不变,将容器的容积扩大为原来的2倍,达到新平衡时测得c(A)为0.22mol/L.下列有关判断对的是( )
| A、x+y>z |
| B、化学反应速率将比原来的更快 |
| C、A、B的转化率减小 |
| D、混合气体的平均摩尔质量变小 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:保持温度不变,将容器的体积扩大两倍,如平衡不移动,A的浓度为0.25mol/L,大于实际A的浓度变为0.22mol/L,说明平衡向消耗A的方向移动,即向正反应移动,据此结合选项解答.
解答:
解:保持温度不变,将容器的体积扩大两倍,如平衡不移动,A的浓度为0.25mol/L,大于实际A的浓度变为0.22mol/L,说明平衡向消耗A的方向移动,即向正反应移动
A、增大体积,压强减小,平衡向正反应移动,压强减小平衡向气体物质的量增大的方向移动,即x+y<z,故A错误;
B、由上述分析可知,体积增大压强减小,反应速率减小,故B错误;
C、平衡向正反应方向移动,AB的转化率增大,故C错误;
D、气体质量不变,平衡正向进行,气体物质的量增大,混合气体的平均摩尔质量变小,故D正确;
故选D.
A、增大体积,压强减小,平衡向正反应移动,压强减小平衡向气体物质的量增大的方向移动,即x+y<z,故A错误;
B、由上述分析可知,体积增大压强减小,反应速率减小,故B错误;
C、平衡向正反应方向移动,AB的转化率增大,故C错误;
D、气体质量不变,平衡正向进行,气体物质的量增大,混合气体的平均摩尔质量变小,故D正确;
故选D.
点评:本题考查化学平衡移动,难度中等,利用假设法判断平衡移动方向是解题关键.

练习册系列答案
相关题目
通常人们把拆开1mol某化学键吸收的能量看成该化学键的键能,如表是一些化学键的键能.
根据键能数据估算下列反应CH4(g)+4F2(g)═CF4(g)+4HF(g)的反应热△H为( )
| 化学键 | C-H | C-F | H-F | F-F |
| 键能/(kJ?mol-1) | 414 | 489 | 565 | 155 |
| A、1940kJ?mol-1 |
| B、-1940kJ?mol-1 |
| C、-485kJ?mol-1 |
| D、485kJ?mol-1 |
有相同pH的三种酸HX、HY、HZ的溶液,稀释相同倍数后,pH的变化值依次增大,则HX、HY、HZ的酸性由强到弱的顺序是( )
| A、HX、HY、HZ |
| B、HZ、HY、HX |
| C、HX、HZ、HY |
| D、HY、HZ、HX |
a mol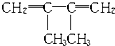 和b mol CH2=CH-CN按一定比例加聚成高分子化合物A.一定量的A完全燃烧生成CO2(g)、H2O(g)和N2(g),其中CO2的体积分数为57.14%,则形成A的两有机物的物质的量比为( )
和b mol CH2=CH-CN按一定比例加聚成高分子化合物A.一定量的A完全燃烧生成CO2(g)、H2O(g)和N2(g),其中CO2的体积分数为57.14%,则形成A的两有机物的物质的量比为( )
 和b mol CH2=CH-CN按一定比例加聚成高分子化合物A.一定量的A完全燃烧生成CO2(g)、H2O(g)和N2(g),其中CO2的体积分数为57.14%,则形成A的两有机物的物质的量比为( )
和b mol CH2=CH-CN按一定比例加聚成高分子化合物A.一定量的A完全燃烧生成CO2(g)、H2O(g)和N2(g),其中CO2的体积分数为57.14%,则形成A的两有机物的物质的量比为( )| A、1:1 | B、1:2 |
| C、2:3 | D、3:4 |
下列现象与盐类水解无关的是( )
| A、将Al粉投入到NaHSO4溶液中,有气泡生成 |
| B、配制FeCl3溶液时适当加入少量盐酸 |
| C、明矾可作净水剂 |
| D、泡沫灭火器用Al2(SO4)3与NaHCO3为原料 |
A、B、C、D是同一周期的四种主族元素,A和B的最高价氧化物对应的水化物显碱性,且碱性B>A;C、D两种元素对应的气态氢化物的稳定性C>D,则它们的原子序数由小到大的顺序是( )
| A、B<A<C<D |
| B、A<B<C<D |
| C、B<A<C<D |
| D、B<A<D<C |
下列常用实验仪器中,不能直接用于混合物的分离或提纯的是( )
| A、分液漏斗 | B、容量瓶 |
| C、蒸馏烧瓶 | D、燃烧匙 |