题目内容
7.有关杂化轨道理论的说法不正确的是( )| A. | 杂化轨道全部参加形成化学键 | |
| B. | 杂化前后的轨道数不变,但轨道的形状发生了改变 | |
| C. | sp3、sp2、sp杂化轨道的夹角分别为109°28′、120°、180° | |
| D. | 四面体形、三角锥形的结构可以用sp3杂化轨道解释 |
分析 A.杂化轨道可以部分参加形成化学键;
B.原子轨道杂化前后轨道总数不变,但形状发生变化;
C.根据其空间构型判断杂化轨道的夹角;
D.采用用sp3杂化的分子根据其含有的孤电子对个数确定其实际空间构型.
解答 解:A.杂化轨道可以部分参加形成化学键,例如NH3中N发生了sp3杂化,形成了4个sp3杂化杂化轨道,但是只有3个参与形成化学键,故A错误;
B.杂化前后的轨道数不变,杂化后,各个轨道尽可能分散、对称分布,导致轨道的形状发生了改变,故B正确;
C.sp3、sp2、sp杂化轨道其空间构型分别是正四面体、平面三角形、直线型,所以其夹角分别为109°28′、120°、180°,故C正确;
D.部分四面体形、三角锥形分子的结构可以用sp3杂化轨道解释,如甲烷、氨气分子,故D正确;
故选A.
点评 本题考查了原子杂化,根据价层电子对互斥理论确定分子空间构型及原子杂化方式的判断,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.在N2+3H2$?_{催化剂}^{高温、高压}$2NH3的反应中,经过一段时间后,NH3的浓度增加了0.6mol•L-1.在此时间内用H2表示的平均反应速率为0.45mol•L-1•s-1,所经过的时间是( )
| A. | 0.44 s | B. | 1 s | C. | 1.33 s | D. | 2 s |
18.铁钉和碳棒用导线连接后,浸入0.01mol\l的食盐溶液中,可发生的反应是( )
| A. | 碳棒上放出氯气 | B. | 铁钉上放出氢气 | C. | 碳棒上放出氧气 | D. | 铁钉锈蚀 |
15.检验久置的FeSO4是否变质,最好选用的试剂是( )
| A. | 铁片 | B. | NaOH溶液 | C. | 石蕊溶液 | D. | KSCN溶液 |
2.如表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:(无特殊说明均填元素符号、化学式等化学用语)
(1)在这些元素中,化学性质最不活泼的元素是Ne,元素原子半径最大的是K,
(2)在上述元素的最高价氧化物对应水化物中,酸性最强的化合物的化学式是HClO4,碱性最强的化合物的化学式是KOH,既能与强酸反应,又能与强碱反应的化合物的化学式是Al(OH)3.
(3)比较⑦、⑧、⑨、⑩四种元素的简单离子的离子半径从大到小的顺序是S2->Cl->K+>Al 3+(用离子符号表示).
(4)⑤和③形成的A2B2型化合物的电子式为 ,属于离子化合物(填“离子化合物”还是“共价化合物”).
,属于离子化合物(填“离子化合物”还是“共价化合物”).
(5)写出能证明⑨元素的非金属性比⑧强的一个化学方程式:H2S+Cl2=2HCl+S.
| 主族 周期 | IA | ⅡA | IIIA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
| 4 | ⑩ |
(2)在上述元素的最高价氧化物对应水化物中,酸性最强的化合物的化学式是HClO4,碱性最强的化合物的化学式是KOH,既能与强酸反应,又能与强碱反应的化合物的化学式是Al(OH)3.
(3)比较⑦、⑧、⑨、⑩四种元素的简单离子的离子半径从大到小的顺序是S2->Cl->K+>Al 3+(用离子符号表示).
(4)⑤和③形成的A2B2型化合物的电子式为
 ,属于离子化合物(填“离子化合物”还是“共价化合物”).
,属于离子化合物(填“离子化合物”还是“共价化合物”).(5)写出能证明⑨元素的非金属性比⑧强的一个化学方程式:H2S+Cl2=2HCl+S.
12.实验室用下图所示装置制备氯气并进行一系列相关的实验(夹持设备已省略).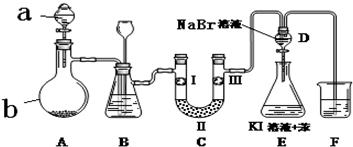
(1)a、b两仪器的名称:a分液漏斗;b蒸馏烧瓶.
(2)洗气装置B是为了除去Cl2中的HCl气体,应放入的试剂是饱和食盐水;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象B中长颈漏斗中液面上升,形成水柱.
(3)制备氯气选用的药品为:漂粉精固体【主要成分为Ca(ClO)2】和浓盐酸,相关的化学反应方程式为Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O.
(4)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入c.
(5)设计装置D、E的目的是比较氯、溴、碘的非金属性.当向D中缓缓通入一定量氯气时,可以看到无色溶液逐渐变为黄色,说明氯的非金属性大于溴(填“大于”或“小于”).
(6)F处为烧碱溶液,写出吸收Cl2的离子方程式Cl2+2OH-=Cl-+ClO-+H2O.

(1)a、b两仪器的名称:a分液漏斗;b蒸馏烧瓶.
(2)洗气装置B是为了除去Cl2中的HCl气体,应放入的试剂是饱和食盐水;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象B中长颈漏斗中液面上升,形成水柱.
(3)制备氯气选用的药品为:漂粉精固体【主要成分为Ca(ClO)2】和浓盐酸,相关的化学反应方程式为Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O.
(4)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入c.
| a | b | c | d | |
| I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| II | 碱石灰 | 硅胶 | 无水氯化钙 | 浓硫酸 |
| III | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(6)F处为烧碱溶液,写出吸收Cl2的离子方程式Cl2+2OH-=Cl-+ClO-+H2O.
19.糖类、油脂、蛋白质是维持人体生命活动所必需的三大营养物质.下列说法你认为正确的是( )
①淀粉是人体所需能量的主要来源,可以用碘水检验淀粉
②油脂可以在酸性条件下水解生成甘油和肥皂
③部分蛋白质遇到浓硝酸会变黄
④甘蔗中含有蔗糖,它和麦芽糖互为同分异构体
⑤糖类、油脂和蛋白质都能发生水解.
①淀粉是人体所需能量的主要来源,可以用碘水检验淀粉
②油脂可以在酸性条件下水解生成甘油和肥皂
③部分蛋白质遇到浓硝酸会变黄
④甘蔗中含有蔗糖,它和麦芽糖互为同分异构体
⑤糖类、油脂和蛋白质都能发生水解.
| A. | ②③④ | B. | ①③⑤ | C. | ①③④ | D. | ②④⑤ |
17.下列叙述不正确的是( )
| A. | 过氧化氢中既含有极性键又含有非极性键 | |
| B. | 18O原子中含有18个中子 | |
| C. | 含有相同电子数的H2O和NH3的分子数相同 | |
| D. | 苯分子中所有原子共处在同一平面上 |