题目内容
12.某学生对碱性工业废水样品进行研究,其实验操作或结论的描述,正确的是( )| A. | 将废水加入紫色石蕊试剂中检验酸碱性 | |
| B. | 用玻璃棒蘸取废水样品,蘸在润湿的pH试纸上测定其pH | |
| C. | 测得该废水样品的pH=10,则废水样品中c(OH-)=10-10 mol/L | |
| D. | 该工业废水中c(H+)<c(OH-) |
分析 A.用指示剂检验溶液酸碱性,应将指示剂滴加到待测液中;
B.依据pH试纸使用方法解答;
C.pH=10,说明c(H+)=10-10 mol•L-1;
D.溶液呈碱性则氢离子浓度小于氢氧根离子浓度.
解答 解:A.检验废水酸碱性,应向待测液样品中滴加紫色石蕊试纸,故A错误;
B.使用pH试纸检测溶液pH值,不能润湿,故B错误;
C.pH=10,说明c(H+)=10-10 mol•L-1,故C错误;
D.pH=10说明溶液呈碱性,则氢离子浓度小于氢氧根离子浓度,故D正确;
故选:D.
点评 本题考查试纸的使用、指示剂的使用、pH的简单计算,为高频考点,侧重于基本理论的理解和应用的考查,注意相关基础知识的积累,难度不大

练习册系列答案
相关题目
3.下列说法正确的是( )
| A. | O2和O2互为同位素,化学性质相似 | |
| B. | 水是一种非常稳定的化合物,这是由于氢键所致 | |
| C. | 分子晶体中一定存在分子间作用力,但可能没有共价键 | |
| D. | 将标准状况下22.4 L 氨气溶于1 L水配成溶液,可得1 mol•L-1的氨水 |
7.下列有关溶液组成的描述合理的是( )
| A. | 无色溶液中可能大量存在Al3+、NH4+、Cl?、S2- | |
| B. | 使酚酞变红的溶液中可能大量存在Na+、ClO?、SO42-、I? | |
| C. | 碱性溶液中可能大量存在Na+、K+、HCO3?、CO32- | |
| D. | 中性溶液中可能大量存在Fe3+、K+、SCN-、SO42- |
17.设NA为阿伏加德罗常数的值,下列说法不正确的是( )
| A. | 标准状况下,22.4L乙醇含有2NA个碳子 | |
| B. | 常温常压下,17g羟基含有9NA个电子 | |
| C. | 28g乙烯和丙烯(C3H6)的混合气体中含有的碳原子数为2NA | |
| D. | 1molNa被完全氧化生成Na2O2,失去NA个电子 |
1.秦皮素具有抗痢疾杆菌功效,其结构如图所示,下列有关说法正确的是( )


| A. | 秦皮素分子中有三种类型的官能团 | |
| B. | 1mol秦皮素与过量浓溴水反应时,消耗2molBr2 | |
| C. | 1mol秦皮素最多与3molNaOH发生反应 | |
| D. | 1mol秦皮素最多与5molH2加成 |
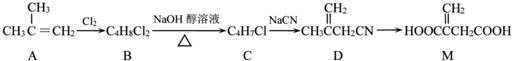
 +NaOH$→_{△}^{乙醇}$
+NaOH$→_{△}^{乙醇}$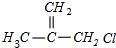 +NaCl+H2O,其反应类型为消去反应.
+NaCl+H2O,其反应类型为消去反应.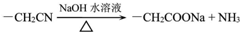 ,D经五步转成变成M的合成反应流程为:
,D经五步转成变成M的合成反应流程为: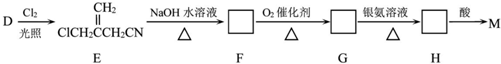
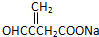 ;
;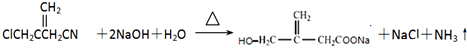 ;
;
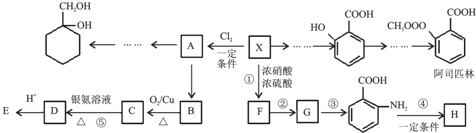
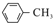 $\stackrel{KMnO_{4}/H+}{→}$
$\stackrel{KMnO_{4}/H+}{→}$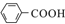
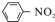 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$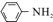 (苯胺,易被氧化)
(苯胺,易被氧化) ,分子中最多有13个原子共面.
,分子中最多有13个原子共面. .
. .
.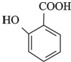 有多种同分异构体,试写出所有苯环上含有1个醛基和2个羟基,且核磁共振氢谱显示为4组峰的芳香族化合物的结构简式
有多种同分异构体,试写出所有苯环上含有1个醛基和2个羟基,且核磁共振氢谱显示为4组峰的芳香族化合物的结构简式 .
. 最合理的方案.在合成路线流程图的方框中填出相应的物质,并在括号注明反应条件.
最合理的方案.在合成路线流程图的方框中填出相应的物质,并在括号注明反应条件.
 B.
B.  C.
C.  D.
D. 