题目内容
16.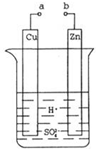 原电池是化学对人类的一项重大贡献.某兴趣小组为研究原电池原理,设计如图装置.
原电池是化学对人类的一项重大贡献.某兴趣小组为研究原电池原理,设计如图装置.(1)a和b用导线连接,Cu极为原电池正极极(填“正”或“负”),电极反应式是2H++2e-=H2↑.Zn极发生氧化(填“氧化”或“还原”)反应.溶液中H+移向Cu(填“Cu”或“Zn”)极.
(2)无论a和b是否连接,Zn片均被腐蚀.若转移了0.2mol电子,则理论上Zn片质量减轻了6.5gg.(已知Zn的相对原子质量为65)
分析 (1)a和b用导线连接,该装置构成原电池,锌失电子发生氧化反应而作负极,铜作正极,正极上氢离子得电子发生还原反应,电解质溶液中阳离子向正极移动;
(2)根据锌与转移电子之间的关系式计算.
解答 解:(1)a和b用导线连接,该装置构成原电池,铜作正极,正极上氢离子得电子发生还原反应,电极反应式为2H++2e-=H2↑;锌失电子发生氧化反应而作负极,放电时,电解质溶液中氢离子向正极铜电极移动,
故答案为:正;2H++2e-=H2↑;氧化;Cu;
(2)负极电极反应为:Zn-2e-=Zn2+,锌片减少的质量=$\frac{0.2mol}{2}$×65g/mol=6.5g,
故答案为:6.5.
点评 本题考查原电池原理、氧化还原反应的有关计算等知识点,明确原电池电极反应式的书写是解题关键,比较简单.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
6.下列说法正确的是( )
| A. | 化学反应的能量变化都表现为热量的变化 | |
| B. | 任何化学反应都伴有能量的变化 | |
| C. | 反应物的总能量低于生成物的总能量时,发生放热反应 | |
| D. | 反应物的总能量高于生成物的总能量时,发生吸热反应 |
7.标准状况下,使NO2和O2按4:1体积比充满干燥烧瓶,将烧瓶倒置于水中,瓶内液面逐渐上升,假设烧瓶内溶液不扩散,则最终该溶液中溶质的物质的量浓度为( )
| A. | $\frac{1}{14}$mol/L | B. | $\frac{4}{5}$mol/L | C. | $\frac{1}{28}$mol/L | D. | $\frac{1}{42}$mol/L |
4.短周期元素W、X、Y、Z在元素周期表中的位置如图所示.下列说法正确的是( )


| A. | Z的气态氢化物的稳定性在同主族元素中最强 | |
| B. | W的最高价氧化物对应的水化物是强酸 | |
| C. | W的非金属性比Z的弱 | |
| D. | Y的原子半径在同周期主族元素中最大 |
11.下列化学用语表述正确的是( )
| A. | 质子数为53、中子数为78的碘原子:131 53I | |
| B. | 乙烯的结构简式:CH2CH2 | |
| C. | 一个D2O分子所含的中子数为8 | |
| D. | N2的电子式:N:::N: |
8.下列叙述中,正确的是( )
| A. | pH=3的盐酸中,其c(H+)是pH=1的盐酸中的3倍 | |
| B. | 1mol/L0.5L的 AlCl3溶液中,阳离子的物质的量大于0.5mol | |
| C. | 同温度同物质的量浓度时,HF比HCN易电离,则NaF溶液的 pH 比 NaCN 溶液大 | |
| D. | 在由水电离出的c(H+)=1×10-12mol/L的溶液中,K+、ClO-、SO42-一定能大量共存 |
5.下列各组离子在溶液中能大量共存,加入Fe2(SO4)3后仍能大量共存的是( )
| A. | Na+、I-、CO${\;}_{3}^{2-}$、ClO- | B. | Fe2+、H+、K+、NO${\;}_{3}^{-}$ | ||
| C. | Ba2+、Na+、SCN-、Cl- | D. | Cu2+、Fe2+、Cl-、NO${\;}_{3}^{-}$ |
18.某兴趣小组做了“以铜为电极电解饱和食盐水”实验探究电解原理,装置如图所示.实验现象:接通电源30s内,阳极附近出现白色浑浊,之后变成橙黄色浑浊,此时测定溶液的pH约为10,一段时间后,试管底部聚集大量红色沉淀,溶液仍为无色.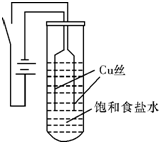
查阅资料(已知:相同温度下CuCl的溶解度大于CuOH),下列说法错误的是( )

| 物质 | 氯化铜 | 氧化亚铜 | 氢氧化亚铜 (不稳定) | 氯化亚铜 |
| 颜色 | 固体呈棕色,浓溶液呈绿色,稀溶液呈蓝色 | 红色 | 橙黄色 | 白色 |
| A. | 电解过程中氯离子向阳极移动 | B. | 电解开始时阳极Cu 放电生成Cu2+ | ||
| C. | 阴极反应为2H2O+2e-=H2↑+2OH- | D. | 随溶液pH升高CuCl逐渐转化为CuOH |
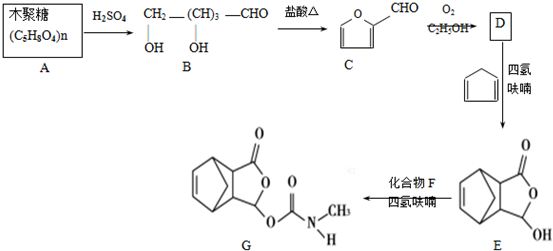
 ,在流程中作反应的催化剂;
,在流程中作反应的催化剂; ;
;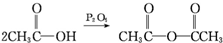 .
. 、CH3NHCOOH.
、CH3NHCOOH. .
. .
.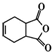 )是合成抗病毒药物阿昔洛韦的中间体.参照上述合成路线,写出以1,3-丁二烯为原料制备H的合成路线流程图(无机试剂任用):
)是合成抗病毒药物阿昔洛韦的中间体.参照上述合成路线,写出以1,3-丁二烯为原料制备H的合成路线流程图(无机试剂任用): .
.