题目内容
14.有Fe2(SO4)3和CuCl2的混合溶液V L将它分成两份.一份滴加氢氧化钠溶液,使Fe3+和Cu2+完全沉淀;另一份滴加Ba(NO3)2溶液,使SO42-完全沉淀.反应中消耗a mol NaOH、b mol Ba(NO3)2.据此得知原混合溶液中c(Cu2+)(单位:mol/L)为( )| A. | $\frac{2a-4b}{V}$ | B. | $\frac{2(a-b)}{V}$ | C. | $\frac{a-2b}{V}$ | D. | $\frac{2a-b}{V}$ |
分析 根据消耗硝酸钡的物质的量计算出每份溶液中含有的硫酸根离子的物质的量,从而可知每份溶液中含有铁离子的物质的量,然后结合铁离子、铜离子消耗氢氧化钠的物质的量计算出铜离子的物质的量,最后根据c=$\frac{n}{V}$计算出混合液中铜离子浓度.
解答 解:滴加bmol Ba(NO3)2溶液,使SO42-完全沉淀,则每份溶液中含有硫酸根离子的物质的量为bmol,根据硫酸铁的化学式可知,每份溶液中含有铁离子的物质的量为:bmol×$\frac{2}{3}$=$\frac{2}{3}$bmol,
$\frac{2}{3}$bmol 铁离子完全沉淀消耗氢氧化钠的物质的量为:$\frac{2}{3}$bmol×3=2bmol,则铜离子生成氢氧化铜消耗NaOH的物质的量为:amol-2bmol=(a-2b)mol,铜离子的物质的量为0.5(a-2b)mol
每份溶液的体积为0.5VL,则混合液中铜离子的浓度为:=$\frac{0.5(a-2b)mol}{0.5VL}$=$\frac{a-2b}{V}$mol/L,
故选C.
点评 本题考查了物质的量浓度的计算、混合物反应的计算,题目难度中等,明确发生反应的原理为解答关键,注意掌握物质的量浓度的概念及表达式,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
4.在下面的反应中,氨作为氧化剂参加反应的是( )
| A. | NH3+H3PO4═NH4H2PO4 | |
| B. | 4NH3+5O2$\frac{\underline{\;\;\;高温\;\;\;}}{催化剂}$4NO+6H2O | |
| C. | 2NH3+3Cl2═6HCl+N2 | |
| D. | NH3+NaH═NaNH2+H2↑ |
5.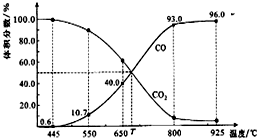 一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)?2CO(g).平衡时,体系中气体体积分数与温度的关系如下图所示.下列说法正确的是( )
一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)?2CO(g).平衡时,体系中气体体积分数与温度的关系如下图所示.下列说法正确的是( )
 一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)?2CO(g).平衡时,体系中气体体积分数与温度的关系如下图所示.下列说法正确的是( )
一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)?2CO(g).平衡时,体系中气体体积分数与温度的关系如下图所示.下列说法正确的是( )| A. | 550℃时,若充入惰性气体,v正,?逆均减小,平衡不移动 | |
| B. | 650℃时,反应达平衡后CO2的转化率为25.0% | |
| C. | T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动 | |
| D. | 该反应为放热反应 |
2.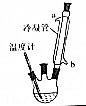 肉桂酸乙酯具有草莓香味,用于配置香水、香精和人造精油.实验室制备肉桂酸乙酯的反应、装置示意图和有关数据如下:
肉桂酸乙酯具有草莓香味,用于配置香水、香精和人造精油.实验室制备肉桂酸乙酯的反应、装置示意图和有关数据如下:
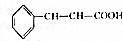 +CH3CH2OH$?_{△}^{浓硫酸}$
+CH3CH2OH$?_{△}^{浓硫酸}$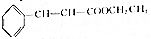 +H2O
+H2O
实验步骤:
制取:①在三颈烧瓶中加入20.0g肉桂酸、50.0g乙醇、数滴浓硫酸和2~3片碎瓷片.开始缓慢加热至约75℃,回流12h.②进行蒸馏.③进行减压蒸馏,精制.最终制得17.6g肉桂酸乙酯.
(1)步骤①中冷凝管的作用是冷凝回流.
(2)步骤②中进行蒸馏的目的是除去乙醇,制备过程中需要控制温度在75℃,常采用的方法是水浴加热.
(3)本实验中加入过量乙醇的目的是提高肉桂酸的转化率.
(4)若要分离肉桂酸乙酯和水的混合物,常采用的分离方法是分液,分离过程中需要用到的玻璃仪器有分液漏斗.下图给出蒸馏操作中,仪器选择及安装都正确的是D(填字母序号).

(5)本实验中肉桂酸的利用率是74%.
 肉桂酸乙酯具有草莓香味,用于配置香水、香精和人造精油.实验室制备肉桂酸乙酯的反应、装置示意图和有关数据如下:
肉桂酸乙酯具有草莓香味,用于配置香水、香精和人造精油.实验室制备肉桂酸乙酯的反应、装置示意图和有关数据如下: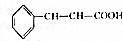 +CH3CH2OH$?_{△}^{浓硫酸}$
+CH3CH2OH$?_{△}^{浓硫酸}$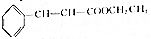 +H2O
+H2O | 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 水中溶解性 | |
| 乙醇 | 46 | 0.789 | 78.3 | 与水互溶 |
| 肉桂酸 | 148 | 1.245 | 300 | 微溶于水 |
| 肉桂酸乙酯 | 176 | 1.049 | 270 | 不溶于水 |
制取:①在三颈烧瓶中加入20.0g肉桂酸、50.0g乙醇、数滴浓硫酸和2~3片碎瓷片.开始缓慢加热至约75℃,回流12h.②进行蒸馏.③进行减压蒸馏,精制.最终制得17.6g肉桂酸乙酯.
(1)步骤①中冷凝管的作用是冷凝回流.
(2)步骤②中进行蒸馏的目的是除去乙醇,制备过程中需要控制温度在75℃,常采用的方法是水浴加热.
(3)本实验中加入过量乙醇的目的是提高肉桂酸的转化率.
(4)若要分离肉桂酸乙酯和水的混合物,常采用的分离方法是分液,分离过程中需要用到的玻璃仪器有分液漏斗.下图给出蒸馏操作中,仪器选择及安装都正确的是D(填字母序号).

(5)本实验中肉桂酸的利用率是74%.
9.如图所示的A、B、C、D、E五种物质的相互关系,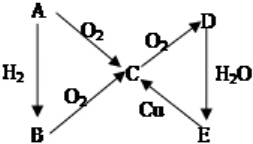 (有些反应条件均已省略,如加热、点燃等)则A的化学式可能是( )
(有些反应条件均已省略,如加热、点燃等)则A的化学式可能是( )
 (有些反应条件均已省略,如加热、点燃等)则A的化学式可能是( )
(有些反应条件均已省略,如加热、点燃等)则A的化学式可能是( )| A. | N2 | B. | Cl2 | C. | S | D. | C |
1.短周期主族元素A、B、C、D、E的原子序数依次递增,A的单质在常温下呈气态,D元素的单质既能与盐酸反应也能与NaOH溶液反应,B、C、E原子的最外层电子数之和为13,E原子的最外层电子数是B原子内层电子数的3倍或是C原子最外层电子数的3倍.下列说法正确的是( )
| A. | 原子半径的大小顺序:r(B)<r(C)<r(D) | |
| B. | 元素B、E的最高价氧化物的水化物都是强酸 | |
| C. | C、D的氧化物都能与氢氧化钠反应 | |
| D. | 工业上常用电解元素C、D的氯化物来制取它们的单质 |
5.下列实验操作中错误的是( )
| A. | 食盐水蒸发结晶,蒸发皿中出现大量晶体时停止加热,利用余热使溶液蒸干 | |
| B. | 金属钠着火,立即用沙土扑灭 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 实验室制取蒸馏水的装置中,冷水从冷凝管的上口进,下口出 |
6.下列对晶体类型判断正确的是( )
| 选项 | Na2B2O7 | CaF2 | H3BO3 | NH3 |
| A | 原子晶体 | 金属晶体 | 原子晶体 | 分子晶体 |
| B | 离子晶体 | 分子晶体 | 离子晶体 | 分子晶体 |
| C | 离子晶体 | 离子晶体 | 分子晶体 | 分子晶体 |
| D | 分子晶体 | 离子晶体 | 分子晶体 | 离子晶体 |
| A. | A | B. | B | C. | C | D. | D |
