题目内容
 如图是目前世界上比较先进的电解饱和食盐水制碱技术--离子交换膜.分别写出①、④、⑤各表示什么物质:
如图是目前世界上比较先进的电解饱和食盐水制碱技术--离子交换膜.分别写出①、④、⑤各表示什么物质:①
考点:电解原理
专题:电化学专题
分析:该交换膜是阳离子交换膜,电解氯化钠溶液时,阳极上氯离子放电生成氯气,所以气体①是Cl2,⑤是饱和NaCl溶液,③是NaCl稀溶液,Na+向阴极室移动,阴极上氢离子放电生成氢气,所以气体②是氢气,生成的NaOH从④排出,阴极上氢离子放电应该加入水,所以⑤是水.
解答:
解:该交换膜是阳离子交换膜,电解氯化钠溶液时,阳极上氯离子放电生成氯气,电极反应式为2Cl--2e-=Cl2↑,所以气体①是Cl2,要使氯离子放电,则加入的溶液应该是饱和氯化钠溶液,所以⑤是饱和NaCl溶液,③是NaCl稀溶液;
Na+向阴极室移动,阴极上氢离子放电生成氢气,电极反应式为2H++2e-=H2↑,所以气体②是氢气,生成的NaOH从④排出,阴极上氢离子放电应该加入水,所以⑤是水,
故答案为:氯气;NaOH溶液;饱和氯化钠溶液.
Na+向阴极室移动,阴极上氢离子放电生成氢气,电极反应式为2H++2e-=H2↑,所以气体②是氢气,生成的NaOH从④排出,阴极上氢离子放电应该加入水,所以⑤是水,
故答案为:氯气;NaOH溶液;饱和氯化钠溶液.
点评:本题考查电解原理,根据阴阳极上放电的离子确定加入的物质、排出溶液及生成气体成分,题目难度不大.

练习册系列答案
相关题目
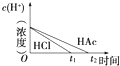
25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A、0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积混合:c(Na+)=c(Cl-)>c(CH3COO-)>c(H+)>c(OH-) | ||
| B、0.1mol/LH2SO4与0.1mol/L氨水等体积混合:c(H+)>c(NH4+)>c(SO42-)>c(OH-) | ||
C、0.1mol/LNa2CO3与0.1mol/L NaHCO3溶液等体积混合:
| ||
| D、0.1mol/LNa2C2O4与0.1mol/LHCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+) |
下列物质分类正确的是( )
A、 芳香族化合物 芳香族化合物 |
B、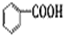 羧酸 羧酸 |
C、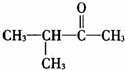 醛 醛 |
D、 酚 酚 |
下列有关叙述中正确的是( )
| A、因为s轨道的形状是球形的,所以s电子做的是圆周运动 |
| B、3px、3py、3pz的差异之处在于三者中电子(基态)的能量不同 |
| C、原子轨道和电子云都是用来形象地描述电子运动状态的 |
| D、H2、F2、HCl和H2O中的σ键都是sp σ键 |
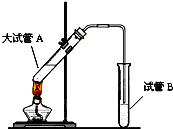 在实验室,可以用如图所示的装置制取乙酸乙酯.请回答下列问题:
在实验室,可以用如图所示的装置制取乙酸乙酯.请回答下列问题: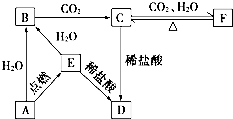 如图所示,下列各项变化的未知物焰色反应均呈黄色,E为淡黄色粉末.回答下列问题.
如图所示,下列各项变化的未知物焰色反应均呈黄色,E为淡黄色粉末.回答下列问题.