题目内容
2.用0.1mol的氯化钠固体配成溶液500mL,所得溶液的物质的量浓度为( )| A. | 0.1mol/L | B. | 0.2mol/L | C. | 0.3mol/L | D. | 0.4mol/L |
分析 用0.1mol的氯化钠固体配成溶液500mL,根据物质的量浓度表达式c=$\frac{n}{V}$计算出所得溶液的物质的量浓度.
解答 解:用0.1mol的氯化钠固体配成溶液500mL,所得溶液的物质的量浓度为:c(NaCl)=$\frac{0.1mol}{0.5L}$=0.2mol/L,
故选B.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确物质的量浓度的概念及表达式为解答关键,试题侧重基础知识的考查,培养学生的化学计算能力.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
12.有关甲烷的叙述错误的是( )
| A. | 甲烷分子中的原子都在同一平面内 | |
| B. | 通常情况下,甲烷与强酸、强碱、强氧化剂不起反应 | |
| C. | 光照下,甲烷与氯气发生的是取代反应 | |
| D. | 甲烷的氯化物都难溶于水 |
13.在2L密闭容器中进行如下反应:N2+3H2$?_{催化剂}^{高温高压}$2NH3,5min内氨的物质的量增加了0.1mol,则反应速率为( )
| A. | v(NH3)=0.02mol•(L•min)-1 | B. | v(NH3)=0.01mol•(L•min)-1 | ||
| C. | v(N2)=0.01mol•(L•min)-1 | D. | v(H2)=0.03mol•(L•min)-1 |
10.下列给出的有机物属于饱和烃的为( )
| A. | CCl4 | B. | C2H6 | C. | CH4 | D. | H2C═CH2 |
17.区别溶液和胶体最简单的方法( )
| A. | 加热 | B. | 丁达尔效应 | C. | 电泳 | D. | 观察外观 |
7.反应4A(g)+3B(g)?2C(g)+D(g),达到平衡时,下列说法正确的是( )
| A. | A、B全部变成了C和D | B. | B的正反应速率和逆反应速率相等 | ||
| C. | 反应已经停止 | D. | A、B、C、D四种物质的浓度一定相等 |
14.氡(Rn)是放射性元素,某些建筑材料中若含有氡,将对人体健康造成危害.222Rn来自镭而称之为镭射气,220Rn来自钍而称之为钍射气,219Rn来自锕而称之为锕射气.下列有关氡的说法正确的是( )
| A. | 氡气是双原子分子 | |
| B. | 氡气因其化学性质活泼而对人体有害 | |
| C. | 氡元素有222Rn、220Rn、219Rn三种同素异形体 | |
| D. | 氡的原子核外有6个电子层,最外层有8个电子 |
11.下列说法错误的是( )
| A. | 改变压强不一定改变反应速率 | |
| B. | 使用催化剂能同时增大正、逆反应的速率,并改变化学反应的限度 | |
| C. | 固体物质的状态(如块状、粉末状等)对反应速率有影响 | |
| D. | 升高温度一定能增大反应速率 |
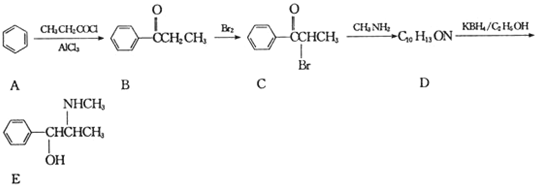
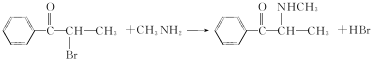 .A→B的反应类型为取代反应.
.A→B的反应类型为取代反应.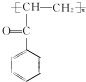 .
.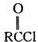
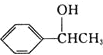 的合成路线:
的合成路线: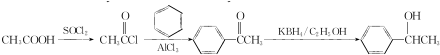 .
.