题目内容
某固体粉末X中可能含有FeO、Fe2O3、MnO2、K2S、K2SO3、KAlO2、MgCl2、K2SO4、K2CO3、NaNO2中的若干种.为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如下: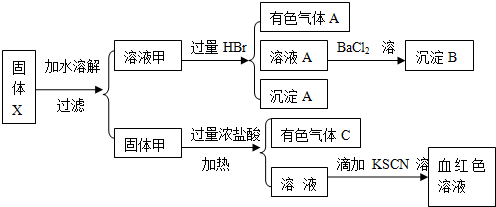 根据上述实验,以下说法正确的是( )
根据上述实验,以下说法正确的是( )
 根据上述实验,以下说法正确的是( )
根据上述实验,以下说法正确的是( )| A、原混合物中一定不含有MgCl2 |
| B、气体A的成分可能超过2种 |
| C、溶液甲中一定含有Na2SiO3、NaNO2、K2SO4可能含有K2CO3、K2SO3 |
| D、固体甲中除MnO2外,可能只含有FeO |
考点:物质的检验和鉴别的实验方案设计
专题:实验设计题
分析:有色气体A应为NO2,可能含有CO2气体,说明一定含有NaNO2,固体甲与浓盐酸反应生成有色气体C,C应为Cl2,则应含有MnO2,沉淀A应为S,说明含有K2S、K2SO3,则一定不含有MgCl2,溶液A和氯化钡反应得到沉淀,沉淀为硫酸钡沉淀,则原溶液含K2SO4,溶液加KSCN溶液呈血红色,说明含有Fe3+,则固体中可能含有FeO、Fe2O3,Fe2+可被氯气氧化生成Fe3+,以此解答该题.
解答:
解:有色气体A应为NO2,可能含有CO2气体,说明一定含有NaNO2,固体甲与浓盐酸反应生成有色气体C,C应为Cl2,则应含有MnO2,沉淀A应为S,说明含有K2S、K2SO3,则一定不含有MgCl2,溶液A和氯化钡反应得到沉淀,沉淀为硫酸钡沉淀,则原溶液含K2SO4,溶液加KSCN溶液呈血红色,说明含有Fe3+,则固体甲中可能含有FeO、Fe2O3,Fe2+可被氯气氧化生成Fe3+,
A.由上述分析可知,一定不含MgCl2,故A正确;
B.有色气体A应为NO2,可能含有CO2气体,不超过2种,故B错误;
C.由以上分析可知溶液甲中一定含有K2S、K2SO3、NaNO2、K2SO4,可能含有K2CO3,也可能含有KAlO2,故C错误;
D.由上述分析可知,固体甲中除MnO2外,可能含有FeO、Fe2O3,故D错误;
故选A.
A.由上述分析可知,一定不含MgCl2,故A正确;
B.有色气体A应为NO2,可能含有CO2气体,不超过2种,故B错误;
C.由以上分析可知溶液甲中一定含有K2S、K2SO3、NaNO2、K2SO4,可能含有K2CO3,也可能含有KAlO2,故C错误;
D.由上述分析可知,固体甲中除MnO2外,可能含有FeO、Fe2O3,故D错误;
故选A.
点评:本题考查物质的检验和鉴别的实验方案的设计,侧重于元素化合物知识的综合运用,题目难度中等,注意把握反应的现象,根据现象结合物质的性质进行判断,易错点为B,注意体会.

练习册系列答案
相关题目
已知电离平衡常数:Ka1(H2CO3)>Ka(HClO)>Ka2(H2CO3),还原性:I->Fe2+>Br-.下列有关判断不正确的是( )
| A、FeCl3溶液滴入KI淀粉溶液后,溶液变蓝 |
| B、纯碱溶液中滴入少量氯水后生成次氯酸、氯化钠等 |
| C、NaClO溶液中通入少量二氧化碳的离子方程式:ClO-+CO2+H2O=HClO+HCO3- |
| D、向FeI2溶液中滴加少量溴水,反应的离子方程式为:2I-+Br2=I2+2Br- |
某无色溶液,其中有可能存在的离子如下:Na+、Ag+、Ba2+、Al3+、AlO2-、S2-、CO32-、SO32-、SO42-.现取该溶液进行有关实验,实验结果如图所示:
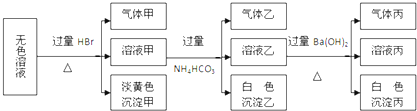
下列说法正确的是( )

下列说法正确的是( )
| A、沉淀甲可能是AgBr |
| B、沉淀丙一定是BaCO3 |
| C、气体甲的成份只有4种可能 |
| D、肯定存在的离子有AlO2-、S2-、SO32-、Na+ |
氢氧化钙溶解度随温度的变化如表所示,下列说法错误的是( )
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 100 | 150 | 200 |
| 溶解度(g/100gH2O) | 0.18 | 0.17 | 0.16 | 0.15 | 0.14 | 0.11 | 0.092 | 0.074 | 0.034 | 0.012 |
| A、氢氧化钙的溶解是放热过程 |
| B、100℃时氢氧化钙的Kxp约等于4×10-6 |
| C、温度升高时氢氧化钙溶解速率加快 |
| D、100℃时pH=12的溶液中c(Ca2+)≤0.04mol?L-1 |
下面提到的问题中,与盐的水解无关的是( )
| A、明矾和FeCl3可作净水剂 |
| B、为保存FeCl3溶液,要在溶液中加少量盐酸 |
| C、用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂 |
| D、氢氟酸用塑料试剂瓶保存而不用玻璃试剂瓶保存 |
 某溶液中可能含有的离子如下表:
某溶液中可能含有的离子如下表: