题目内容
14.某物质可在酸性条件下水解并且生成两种相对分子质量相等的物质,该物质是( )| A. | HCOOC2H5 | B. | CH3COOC2H5 | C. | C6H12O6 | D. | (C6H10O5)n |
分析 A.甲酸乙酯水解生成甲酸和乙醇;
B.乙酸乙酯水解生成乙醇和乙酸;
C.该物质可能是蔗糖或麦芽糖;
D.该物质可能是淀粉或纤维素.
解答 解:A.甲酸乙酯水解生成甲酸和乙醇,甲酸和乙醇的相对分子质量相等,故A正确;
B.乙酸乙酯水解生成乙醇和乙酸,乙酸的相对分子质量大于乙醇,故B错误;
C.该物质可能是蔗糖或麦芽糖,如果是蔗糖,蔗糖水解生成的葡萄糖和果糖的相对分子质量相等,但如果是麦芽糖,麦芽糖水解只生成葡萄糖,故C错误;
D.该物质可能是淀粉或纤维素,淀粉和纤维素最终水解都只生成葡萄糖,故D错误;
故选A.
点评 本题考查有机物结构和性质,为高频考点,侧重考查学生分析判断能力,明确物质结构特点及水解产物成分是解本题关键,注意淀粉和纤维素不是同分异构体,注意蔗糖和麦芽糖水解产物区别,为易错点.

练习册系列答案
相关题目
4.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | lmol的Na2CO3溶于盐酸形成混合溶液1L,常温下在pH=4时,c(CO32-)+c(HCO3-)+c(H2CO3)=0.lmol/L | |
| B. | 标准状况下,2.24 L一氯甲烷中含有氢原子数目为0.3NA | |
| C. | 等物质的量的O2和CO2所含氧原子数均为2NA | |
| D. | 6.8 g熔融的KHSO4中含有0.1 NA个阳离子 |
5.常温下,在pH值为4的FeCl3溶液、pH值为10的Na2CO3溶液和pH值为2的盐酸溶液中,水的电离度分别为α1、α2和α3,则它们的关系为( )
| A. | α1=α2>α3 | B. | α1<α2<α3 | C. | α1>α2>α3 | D. | 无法判断 |
2.下列各组化合物中,化学键的类型相同的是( )
| A. | CO2和NaCl | B. | Na2O和Na2O2 | C. | CaCl2和Na2S | D. | HCl和NaOH |
9.请你观察下列几个装置示意图,有关叙述正确的是( )
| A. |  装置中阳极上析出红色固体 | B. | 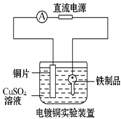 装置中铜片应与电源负极相连 | ||
| C. |  装置中外电路电流方向:b极→a极 | D. |  装中阴极反应:2Cl--2e-═Cl2↑ |
19.下列关于常见有机化合物的说法中正确的是( )
| A. | 乙烷和Cl2在光照条件下反应生成6种氯代产物 | |
| B. | 乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去 | |
| C. | 乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 | |
| D. | 糖类、油脂和蛋白质都是人体必需的营养物质,它们的组成元素相同 |
6.下列属于放热反应的是( )
| A. | 2Na+2H2O═2NaOH+H2↑ | |
| B. | CaCO3 $\frac{\underline{\;高温\;}}{\;}$ CaO+CO2↑ | |
| C. | C+H2O $\frac{\underline{\;高温\;}}{\;}$ CO+H2 | |
| D. | 2NH4Cl+Ba(OH)2•8H2O═BaCl2+2NH3↑+10H2O |
3.短周期元素A、B、C、D的原子序数依次递增,它们的核电荷数之和为32,原子最外层电子数之和为10,A与C同主族,B与D同主族,A、C原子的最外层电子数之和等于B原子的次外层电子数,下列有关叙述正确的是( )
| A. | B、D的最高价氧化物中,B、D与氧原子都形成离子键 | |
| B. | 四种元素的原子半径:A<B<C<D | |
| C. | D元素位于元素周期表中的第三周期第ⅣA族 | |
| D. | 一定条件下,B单质能置换出D单质,C单质能置换出A单质 |
15.下列说法正确的是( )
| A. | 根据反应Cu+H2SO4$\frac{\underline{\;电解\;}}{\;}$CuSO4+H2↑可推出Cu的还原性比H2的强 | |
| B. | 在反应CaH2+2H2O═Ca(OH)2+2H2↑中,水作氧化剂 | |
| C. | 反应3NO2+H2O═2HNO3+NO中氧化剂和还原剂的物质的量之比是3:1 | |
| D. | 因Cl2的氧化性强于I2的氧化性,所以置换反应I2+2NaClO3═2NaIO3+Cl2不能发生 |