题目内容
 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )| A、原子半径:W>Z>Y>X |
| B、含Y元素的盐溶液一定显酸性 |
| C、最简单气态氢化物的热稳定性:Z>W |
| D、X与氢元素组成的化合物XH5与水反应可产生两种气体 |
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:由短周期元素在周期表中的位置可知,X处于第二周期,Y、Z、W处于第三周期,W原子的最外层电子数是最内层电子数的3倍,最外层电子数为6,则W为S,可推知X为N,Y为Al,Z为Si,结合元素周期律及其单质化合物的性质来解答.
解答:
解:由短周期元素在周期表中的位置可知,X处于第二周期,Y、Z、W处于第三周期,W原子的最外层电子数是最内层电子数的3倍,最外层电子数为6,则W为S,可推知X为N,Y为Al,Z为Si,
A.同周期随原子序数增大,原子半径减小,电子层越多,原子半径越大,则原子半径为Y>Z>W>X,故A错误;
B.Y为Al,AlCl3溶液显酸性,NaAlO2溶液显碱性,故B错误;
C.非金属性W>Z,则最简单气态氢化物的热稳定性为W>Z,故C错误;
D.N元素与氢元素组成的化合物XH5为NH4H,NH4H与水反应可产生氨气、氢气两种气体,故D正确,
故选D.
A.同周期随原子序数增大,原子半径减小,电子层越多,原子半径越大,则原子半径为Y>Z>W>X,故A错误;
B.Y为Al,AlCl3溶液显酸性,NaAlO2溶液显碱性,故B错误;
C.非金属性W>Z,则最简单气态氢化物的热稳定性为W>Z,故C错误;
D.N元素与氢元素组成的化合物XH5为NH4H,NH4H与水反应可产生氨气、氢气两种气体,故D正确,
故选D.
点评:本题考查结构性质位置关系应用,W为推断的突破口,注意D选项知识中学基本不接触,为本题难点,注意根据水解反应进行理解,题目难度中等.

练习册系列答案
相关题目
下列电离方程式不正确的是( )
| A、H2SO4═2H++SO42- |
| B、NH4NO3═NH4++NO3- |
| C、Ba(OH)2═Ba2 ++2OH- |
| D、Na2CO3═Na2++CO32- |
下列实验事实不能用平衡移动原理解释的是( )
A、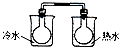 NO2球浸在冷水和热水中 | ||||||||
B、
| ||||||||
C、 | ||||||||
D、
|
阿波罗宇宙飞船以N2H4(联氨)和N2O4为推力源,反应温度达2700℃,反应式为2N2H4+N2O4=3N2+4H2O.关于该反应的说法中正确的是( )
| A、属于置换反应 |
| B、联氨是氧化剂 |
| C、联氨是还原剂 |
| D、氮气是氧化产物,不是还原产物 |
某恒温密闭容器中,可逆反应A(s)?B(?)+C(g)△H=+QKJ/mol(Q>0),达到平衡.缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等.以下分析正确的是( )
| A、产物B的状态可能为气态、固态或液态 |
| B、平衡时,单位时间内m(A)消耗﹕m(C)消耗=1﹕1 |
| C、保持体积不变,向平衡体系中加入B,平衡可能不移动 |
| D、若开始时向容器中加入1molB和1molC,达到平衡时放出热量QKJ |
某温度下,已知反应mX(g)+nY(g)?qZ(g)△H>0,m+n>q,在体积一定的密闭容器中达到平衡,下列叙述正确的是( )
A、反应速率v正(X)=
| ||
B、降低温度,
| ||
| C、增加Y的物质的量,X的转化率减小 | ||
| D、加入X,反应的△H增大 |
下列说法正确的是( )
| A、离子化合物中只能含有离子键 |
| B、共价化合物中只能含有共价键 |
| C、化学键存在于分子之间 |
| D、非极性键只存在于单质中 |
葡萄糖是一种单糖的主要原因是( )
| A、糖类中含碳原子数量最少 |
| B、不能再水解成更简单的糖 |
| C、分子中只有一个醛基 |
| D、糖类中结构最简单 |
 下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加.据此回答问题:
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加.据此回答问题: