��Ŀ����
һ�����룺H2B

H++HB-���������룺HB-

H++B2-
��ش��������⣺
��1��NaHB��Һ______��������ԡ������ʼ��ԡ�����ȷ��������ԭ����______��
��2����0.1mol-L-1��H2B��Һ��ij�¶��µ�pH=3��c��B2-��=1��10-6mol-L-1����H2B��һ������ĵ����Ϊ______��
��3��ij�¶��£���0.1mol-L-1��NaHB��Һ�У����¹�ϵһ������ȷ����______
A��c��H+��-c��OH-��=1��10-14
B��pH��1
C��c��OH-��=2c��H2B��+c��HB-��+c��H+��
D��c��Na+��=0.1mol-L-1��c��B2-��
��4��ij�¶��£�FeB��s��

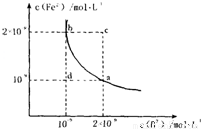
Fe2+��aq��+B2-��aq����ƽ�ⳣ������ʽΪKSP=c��Fe2+��-c��B2-����FeB��ˮ�еij����ܽ�ƽ��������ͼ��ʾ������˵���������______
A��a���Ӧ��KSP����b���Ӧ��KSP
B��d����������
C������ͨ������ʵ����c��䵽a��
D�����¶��£�KSP=4��10-18��

�ʴ�Ϊ����ȷ����NaHB��Һ��ͬʱ����HB��

H++B2-��HB��+H2O

H2B+OH����������ƽ��̶���ȷ����������ȷ����Һ����ԣ�
��2��H2B��Һ��һ������Ϊ��H2B

H++HB-������������HB-

H++B2-��c��B2-��=1��10-6mol?L-1�����Զ����������������Ũ��Ϊ1��10-6mol?L-1������һ���������ɵ�������Ũ��Ϊ1��10-3mol?L-1-1��10-6mol?L-1��1��10-3mol?L-1�����Ե����=
| 1��10-3mol/L |
| 0.1mol/L |
��3��A�������£��κ���Һ�����ӻ�����ʽKw=c��H+��?c��OH-��=1��10-14����������A��ȷ��
B��NaHB��Һ�������Ӳ�����ȫ���룬����0.1mol?L-1��NaHB��Һ��������Ũ��С��0.1mol/L��pH��1����B��ȷ��
C������0.1mol?L-1��NaHB��Һ�е������غ�c��OH-��=c��H2B��-c��B2-��+c��H+������C����
D��c��Na+��=0.1mol?L-1��B2-������������ˮ������ģ�һ����������Ũ��С����D����
��ѡCD��
��4��A��a��b�������ƽ��״̬�ĵ㣬����a���Ӧ��KSP����b���Ӧ��KSP����A��ȷ��
B��d���QcС��KSP�������������ɣ���B��ȷ��
C��c��Qc����KSP�����£������ܽ�ƽ�������ƶ�����Qc�����ᵽa�㣬��C����
D��ȡƽ��̬�µ��κ�һ��a�㣬���¶��£�KSP=2��10-9��10-9=2��10-18����D����
��ѡCD��

 ���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�
���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д� ����ѵ��ϵ�д�
����ѵ��ϵ�д� ��ĩ�����ϵ�д�
��ĩ�����ϵ�д���֪H2B��ˮ��Һ�д������µ��룺
![]()
![]() һ�����룺H2B H++HB-���������룺HB- H++B2-
һ�����룺H2B H++HB-���������룺HB- H++B2-
��ش��������⣺
��1��NaHB��Һ ��������ԡ������ʼ��ԡ�����ȷ��������ԭ����
��
��2����0.1mol��L-1��H2B��Һ��ij�¶��µ�pH=3��c(B2-)=1��10-6mol��L-1����H2B��һ������ĵ����Ϊ ��
��3��ij�¶��£���0.1mol��L-1��NaHB��Һ�У����¹�ϵһ������ȷ���� �� ��
A��c(H+)��c(OH-)=1��10-14
B��pH>1
C��c(OH-)=2c(H2B)+c(HB-)+c(H+)
D��c(Na+)=0.1mol��L-1��c(B2-)
|
��ƽ�ⳣ������ʽΪKSP=c��Fe2+����c��B2-����
FeB��ˮ�еij����ܽ�ƽ����������ͼ��ʾ��
����˵��������ǣ� ��
A��a���Ӧ��KSP����b���Ӧ��KSP
B��d����������
C������ͨ������ʵ����c��䵽a��
D�����¶��£�KSP=4��10-18
��֪H2B��ˮ��Һ�д������µ��룺
![]()
![]() һ�����룺H2B H++HB-���������룺HB- H++B2-
һ�����룺H2B H++HB-���������룺HB- H++B2-
��ش��������⣺
��1��NaHB��Һ ��������ԡ������ʼ��ԡ�����ȷ��������ԭ����
��
��2����0.1mol��L-1��H2B��Һ��ij�¶��µ�pH=3��c(B2-)=1��10-6mol��L-1����H2B��һ������ĵ����Ϊ ��
��3��ij�¶��£���0.1mol��L-1��NaHB��Һ�У����¹�ϵһ������ȷ���� �� ��
A��c(H+)��c(OH-)=1��10-14
B��pH>1
C��c(OH-)=2c(H2B)+c(HB-)+c(H+)
D��c(Na+)=0.1mol��L-1��c(B2-)
|
��ƽ�ⳣ������ʽΪKSP=c��Fe2+����c��B2-����
FeB��ˮ�еij����ܽ�ƽ����������ͼ��ʾ��
����˵��������ǣ� ��
A��a���Ӧ��KSP����b���Ӧ��KSP
B��d����������
C������ͨ������ʵ����c��䵽a��
D�����¶��£�KSP=4��10-18
 ��֪H2B��ˮ��Һ�д������µ��룺
��֪H2B��ˮ��Һ�д������µ��룺 H++HB-���������룺HB-
H++HB-���������룺HB- H++B2-
H++B2- H++B2-��HB?+H2O
H++B2-��HB?+H2O H2B+OH?��������ƽ��̶���ȷ����������ȷ����Һ�����
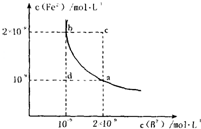
H2B+OH?��������ƽ��̶���ȷ����������ȷ����Һ����� Fe2+��aq��+B2-��aq����ƽ�ⳣ������ʽΪKSP=c��Fe2+��?c��B2-����FeB��ˮ�еij����ܽ�ƽ��������ͼ��ʾ������˵���������
Fe2+��aq��+B2-��aq����ƽ�ⳣ������ʽΪKSP=c��Fe2+��?c��B2-����FeB��ˮ�еij����ܽ�ƽ��������ͼ��ʾ������˵���������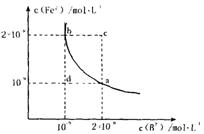
 H++HB-���������룺HB-
H++HB-���������룺HB- H++B2-
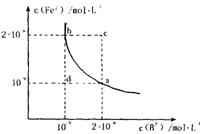
H++B2- Fe2+��aq��+B2-��aq����ƽ�ⳣ������ʽΪKSP=c��Fe2+��?c��B2-����FeB��ˮ�еij����ܽ�ƽ��������ͼ��ʾ������˵���������______
Fe2+��aq��+B2-��aq����ƽ�ⳣ������ʽΪKSP=c��Fe2+��?c��B2-����FeB��ˮ�еij����ܽ�ƽ��������ͼ��ʾ������˵���������______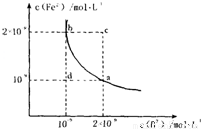
 H++HB-���������룺HB-
H++HB-���������룺HB- H++B2-
H++B2- Fe2+��aq��+B2-��aq����ƽ�ⳣ������ʽΪKSP=c��Fe2+��?c��B2-����FeB��ˮ�еij����ܽ�ƽ��������ͼ��ʾ������˵���������______
Fe2+��aq��+B2-��aq����ƽ�ⳣ������ʽΪKSP=c��Fe2+��?c��B2-����FeB��ˮ�еij����ܽ�ƽ��������ͼ��ʾ������˵���������______