题目内容
8.将一定量的CO2溶于100mL的0.4mol•L-1 KOH溶液.CO2被完全吸收,得到K2CO3和KHCO3的混合溶液.向所得溶液中逐滴加入0.2mol•L-1盐酸,至逸出的CO2与原先吸收的CO2质量相等.此时消耗的盐酸的体积为( )| A. | 100 mL | B. | 200 mL | C. | 300 mL | D. | 400 mL |
分析 将一定量的CO2溶于100mL的0.4mol•L-1 KOH溶液.CO2被完全吸收,得到K2CO3和KHCO3的混合溶液.向所得溶液中逐滴加入0.2mol•L-1盐酸,至逸出的CO2与原先吸收的CO2质量相等,此时相当于CO2没有参与反应,而与KOH溶液反应的是HCl,据此分析.
解答 解:将一定量的CO2溶于100mL的0.4mol•L-1 KOH溶液.CO2被完全吸收,得到K2CO3和KHCO3的混合溶液.向所得溶液中逐滴加入0.2mol•L-1盐酸,至逸出的CO2与原先吸收的CO2质量相等,此时相当于CO2没有参与反应,而与KOH溶液反应的是HCl.
设消耗的盐酸的体积为VL,由KOH和HCl的反应可知:
KOH+HCl=KCl+H2O
1 1
0.4mol/L×0.1L 0.2mol/L×VL
可得:$\frac{1}{0.4mol/L×0.1L}=\frac{1}{0.2mol/L×VL}$
解得V=0.2L=200mL.
故选B.
点评 本题考查了有关方程式的计算,应注意到开始吸收的二氧化碳后来完全逸出,故相当于二氧化碳没有参与反应,实际上和KOH反应的是盐酸.

练习册系列答案
相关题目
18.配制100mL 0.1mol/L的NaCl溶液,下列操作会导致所配溶液浓度偏高的是( )
| A. | 称量时,左盘高,右盘低 | B. | 定容时,俯视读取刻度 | ||
| C. | 容量瓶洗净后未干燥 | D. | 定容时,液面超过了刻度线 |
16.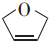 是一种有机烯醚,具有旋光性和吸湿性.下列说法正确的是 ( )
是一种有机烯醚,具有旋光性和吸湿性.下列说法正确的是 ( )
 是一种有机烯醚,具有旋光性和吸湿性.下列说法正确的是 ( )
是一种有机烯醚,具有旋光性和吸湿性.下列说法正确的是 ( )| A. | 分子式为C4H6O | B. | 能使溴水褪色 | C. | 能与钠发生反应 | D. | 能发生消去反应 |
13.有人设计将两根铂丝做电极插入到KOH溶液中,然后在两极上分别通入甲烷和氧气而构成燃料电池.该电池中反应的化学方程式为CH4+2O2+2KOH═K2CO3+3H2O,则关于此燃料电池的下列说法中错误的是 (已知1个电子所带电量为1.6×10-19C)( )
| A. | 通入甲烷的电极为电池的负极,通入氧气的电极为正极 | |
| B. | 在标准状况下,每消耗5.6 L O2,可向外提供2.4×104 C的电量 | |
| C. | 通入甲烷电极的电极反应为:CH4+10OH--8e-═CO32-+7H2O | |
| D. | 放电一段时间后,溶液的pH减小 |
20. X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如表:
X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如表:
(1)Y在元素周期表中的位置是第三周期ⅢA族.
(2)X、Y、Q各自形成简单离子,其中离子半径最大的是O2- (填离子符号).
(3)Q和R按原子个数比1:1组成的化合物甲,是一种“绿色”氧化剂.
①甲的电子式是 .
.
②空气阴极法电解制备甲的装置如图所示.在碱性溶液中,将空气中的氧气还原得到甲和稀碱的溶液,则图中直流电源的a是正极.
 X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如表:
X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如表:| 元素代号 | X | Y | Z | M | Q | R |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 | 0.037 |
| 主要化合价 | +2 | +3 | +6,-2 | +2 | -2 | +1 |
(2)X、Y、Q各自形成简单离子,其中离子半径最大的是O2- (填离子符号).
(3)Q和R按原子个数比1:1组成的化合物甲,是一种“绿色”氧化剂.
①甲的电子式是
 .
.②空气阴极法电解制备甲的装置如图所示.在碱性溶液中,将空气中的氧气还原得到甲和稀碱的溶液,则图中直流电源的a是正极.
17.核潜艇上的核反应堆内使用了液体铝合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是( )
| A. | 离子半径:Na+>Al3+ | |
| B. | 铝钠合金若投入一定水中可得无色溶液并产生气泡 | |
| C. | 若mg不同组成的铝钠合金投入足量盐酸中,若放出的H2越多,则铝的质量分数越少 | |
| D. | 铝钠合金投入到足量氯化铜溶液中,肯定有氢氧化铜沉淀也可能有铜析出 |
18.下列实验操作中正确的是( )
| A. | 分液操作时,先将分液漏斗中下层液体从下口放出,再将上层液体从下口放出 | |
| B. | 萃取操作时,可以选用CCl4或酒精作为萃取剂从溴水中萃取溴单质 | |
| C. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| D. | 蒸馏操作时,应向蒸馏烧瓶中加入几块沸石,以防止暴沸 |
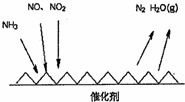 随着我国工业化水平的不断发展,解决水、空气污染问题成为重要课题.
随着我国工业化水平的不断发展,解决水、空气污染问题成为重要课题.