题目内容
4.在自然界里,既有以游离态又有以化合态的形式存在的元素是( )| A. | Cl | B. | P | C. | S | D. | Na |
分析 根据元素的活泼性来判断元素在自然界的存在形式,Cl、P、Na以化合态存在,S既有以游离态又有以化合态存在,据此解答.
解答 解:A.氯气的化学性质活泼,Cl在自然界中只能以化合态存在,故A错误;
B.P的性质活泼,容易与空气中氧气反应,P以化合态存在,故B错误;
C.在自然界中存在单质硫,也存在硫的化合物如硫酸盐等,所以S既以游离态又以化合态存在,故C正确;
D.钠性质活泼,容易与空气中水、氧气反应,Na以化合态存在,故D错误;
故选:C.
点评 本题考查了元素在自然界中的存在形态,题目难度不大,依据元素的活泼性即可判断解答,注意把握常见元素化合物及其单质的性质.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
14.下列有关常见有机物的说法,不正确的是( )
| A. | 天然气和沼气的主要成分都是甲烷,甲烷是一种清洁能源 | |
| B. | 乙烯可以用作果实催熟剂,还可以用于合成有机高分子化合物 | |
| C. | 烷烃和苯通常容易发生取代反应,而烯烃则不能发生取代反应 | |
| D. | 某泸州老窖的瓶子标签上,注明52度,代表100mL该酒水中,含有52mL乙醇 |
15.在NH4Al(SO4)2溶液中,逐滴滴入Ba(OH)2溶液,沉淀的物质的量随Ba(OH)2溶液体积的变化如图,有关分析正确的是( )

| A. | O~M段反应的离子方程式为:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| B. | 沉淀的质量M>P | |
| C. | N点溶液可与Na+、Fe3+、NO3-、Cl-大量共存 | |
| D. | N~P段溶液的pH逐渐减小 |
12.下列反应中,硫酸既表现出强氧化性,又表现出酸性的是( )
| A. | 稀硫酸与锌粒反应生成气体 | B. | 浓硫酸使铁、铝钝化 | ||
| C. | 浓硫酸与铜反应加热反应产生SO2 | D. | 浓硫酸和木炭在加热条件下反应 |
19.关于人造丝和蚕丝的叙述不正确的是( )
| A. | 主要成分都是蛋白质 | B. | 都是高分子化合物 | ||
| C. | 可用灼烧的方法区别二者 | D. | 二者成分不同,但燃烧产物相同 |
9.2SO2(g)+O2(g)$?_{△}^{催化剂}$2SO3(g)是制备硫酸过程中的一步重要反应,下列叙述正确的是( )
| A. | 催化剂不会改变该反应的逆反应速率 | |
| B. | 增大SO2(g)的浓度,逆反应速率会减小 | |
| C. | 该反应是放热反应,降低温度将缩短反应达到平衡的时间 | |
| D. | 在t1、t2时刻,SO3(g)的浓度分别是c1,c2,则时间间隔t1~t2内,SO3(g)生成的平均速率为v=$\frac{{c}_{2}-{c}_{1}}{{t}_{2}-{t}_{1}}$ |
16.某课外兴趣小组对H2O2的分解速率做了如下实验探究.
(1)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据.表中数据为在不同条件下用10mL H2O2制取15OmLO2所需的时间(秒).
①上述实验结果体现了温度、催化剂、浓度等因素对过氧化氢分解速率的影响;
②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对化学反应速率的影响温度升高化学反应速率加快;反应物浓度增大化学反应速率加快;使用合适的催化剂化学反应速率加快.
(2)某温度时,在一个2L的密闭容器中,M、N、W三种气体的物质的量随时间的变化曲线如图所示.根据图中数据.试填写下列空白:
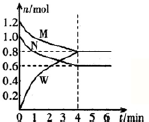
①该反应的化学方程式为M+N?2W.
②从开始至4min,N的平均反应速率为0.05mol/(L•min);4min 末M的转化率为33.3%.
(1)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据.表中数据为在不同条件下用10mL H2O2制取15OmLO2所需的时间(秒).
| 浓度 时间(秒) 反应条件 | 30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 |
| 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加热 | 360 | 480 | 540 | 720 |
| MnO2催化剂、加热 | 10 | 25 | 60 | 120 |
②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对化学反应速率的影响温度升高化学反应速率加快;反应物浓度增大化学反应速率加快;使用合适的催化剂化学反应速率加快.
(2)某温度时,在一个2L的密闭容器中,M、N、W三种气体的物质的量随时间的变化曲线如图所示.根据图中数据.试填写下列空白:

①该反应的化学方程式为M+N?2W.
②从开始至4min,N的平均反应速率为0.05mol/(L•min);4min 末M的转化率为33.3%.