题目内容
13.在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生如下反应:2IO3-+5SO32-+2H+═I2+5SO42-+H2O生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率.某同学设计实验如表所示:
| 0.01mol•L-1 KIO3 酸性溶液(含淀粉)的体积/mL | 0.01mol•L-1 Na2SO3 溶液的体积/mL | H2O的体积 /mL | 实验 温度 /℃ | 溶液出现蓝色时所需时间/s | |
| 实验1 | 5 | V1 | 35 | 25 | |
| 实验2 | 5 | 5 | 40 | 25 | |
| 实验3 | 5 | 5 | V2 | 0 |
分析 依据表中数据判断实验目的,由实验2可以看出混合液的总体积为50mL,V1为10mL,V2为40mL,实验1和实验2可知实验目的是探究该反应速率与亚硫酸钠溶液浓度的关系;实验2和实验3可知实验目的是探究该反应速率与温度的关系.
解答 解:实验1和实验2探究该反应速率与亚硫酸钠溶液浓度的关系,实验2和实验3探究该反应速率与温度的关系;由实验2可以看出混合液的总体积为50mL,V1为10mL,V2为40mL,实验1和实验2可知实验目的是探究该反应速率与亚硫酸钠溶液浓度的关系;实验2和实验3可知实验目的是探究该反应速率与温度的关系,
故答案为:40;实验目的是探究温度、亚硫酸钠溶液浓度与该反应速率的关系.
点评 本题考查了探究该反应速率与溶液浓度、温度的关系,关键在于读表获取信息,注意对比实验中条件的统一,培养学生分析问题、解决问题能力.

练习册系列答案
相关题目
3.“嫦娥一号”月球探测卫星在西昌卫星发射中心由“长征三号甲”运载火箭发射升空.卫星发射后,经过调相轨道段、地月转移轨道段和环月轨道段飞行,已经开始成功执行科学探测任务.“长征三号甲”运载火箭的第一、二级发动机的燃料为偏二甲肼(C2N2H8),四氧化二氮(N2O4)为氧化剂,发生的化学反应是:C2N2H8+2N2O4═2CO2+4H2O+3N2+Q(Q>0).以下说法正确的是( )
| A. | 上述反应中生成的N2是火箭燃料燃烧后的氧化产物 | |
| B. | 推动火箭飞行的强大动力源于该反应瞬间产生的大量高温气体 | |
| C. | 火箭发射时看到的红棕色气体是火箭起飞后,保险活动门自动开启,排出部分高压氧化剂在空气中氧化的结果 | |
| D. | 从能量变化上看,上述反应是热能转化为动能 |
8.分子里所有原子都在同一平面上的是( )
| A. | 甲烷、乙烯、乙炔 | B. | 乙烯、苯、乙炔 | C. | 乙醇、乙醛、乙酸 | D. | 乙烯、苯、甲苯 |
18.具有真正意义上的元素周期表是由哪位化学家发现的是( )
| A. | 门捷列夫(俄国) | B. | 依马林(俄国) | ||
| C. | 别洛索夫(俄国) | D. | 马尔柯夫尼可夫(俄国) |
2.下列叙述中正确的是( )
| A. | 离子化合物中一定含有金属元素 | |
| B. | 分子晶体、原子晶体中一定含有共价键,离子晶体一定含有离子键 | |
| C. | 气态氢化物的稳定性:NH3>PH3>AsH3 | |
| D. | 正四面体结构的分子中的键角一定是109°28′ |
3.固体粉末X中可能含有FeO、Fe2O3、MnO2、K2SiO3、K2SO3、KAlO2、MgCl2、K2CO3、NaNO2中的若干种.为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如图:

根据上述实验,以下说法正确的是( )

根据上述实验,以下说法正确的是( )
| A. | 由现象1和现象3推测溶液甲中一定含有K2SiO3、NaNO2 | |
| B. | 由于在溶液甲中加入足量稀盐酸后再加入BaCl2溶液,因此无法判断溶液中是否有K2SO3 | |
| C. | 无法判断原混合物中是否含有KAlO2、K2CO3、MgCl2 | |
| D. | 根据现象5推测原混合物中一定含有Fe2O3 |
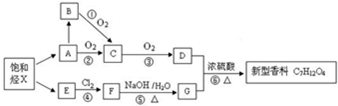
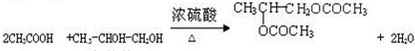
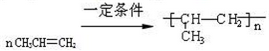
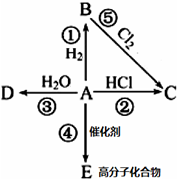 某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A在一定条件下可发生如图所示的转化,请回答下列问题:
某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A在一定条件下可发生如图所示的转化,请回答下列问题: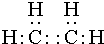 ,其中所含化学键的类型为共价键,E的结构简式为
,其中所含化学键的类型为共价键,E的结构简式为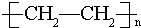 .
.
 .
. .
.