题目内容
下列关于电解质的叙述正确的是( )
| A、CaCO3在水中溶解度很小,所以CaCO3是弱电解质 |
| B、若某种电解质溶液中含有未电离的分子,则该电解质一定是弱电解质 |
| C、氯气和氨气的水溶液导电性都很好,所以它们是电解质 |
| D、SO3的水溶液可以导电,但它不是电解质 |
考点:电解质与非电解质
专题:电离平衡与溶液的pH专题
分析:A、碳酸钙溶于水的部分完全电离,碳酸钙为强电解质;
B、浓硫酸中仅含有少量的水,故硫酸分子不能完全电离;
C、氯气为单质,不属于电解质和非电解质;氨气不能电离出离子;
D、三氧化硫溶于水生成硫酸,硫酸导电.
B、浓硫酸中仅含有少量的水,故硫酸分子不能完全电离;
C、氯气为单质,不属于电解质和非电解质;氨气不能电离出离子;
D、三氧化硫溶于水生成硫酸,硫酸导电.
解答:
解:A、电解质强弱与溶液导电性没有必然关系,强弱电解质的根本区别在于能否完全电离,碳酸钙溶于水的部分完全电离,所以碳酸钙为强电解质,故A错误;
B、浓硫酸中仅含有少量的水,故硫酸分子不能完全电离,但是硫酸属于强电解质,故B错误;
C、氯气为单质,所以既不是电解质,也不是非电解质;氨气的水溶液导电,导电的离子是一水合氨电离的,不是氨气本身电离的,所以氨气为非电解质,故C错误;
D、三氧化硫溶于水生成硫酸,溶液和是硫酸导电,故三氧化硫是非电解质,故D正确,
故选D.
B、浓硫酸中仅含有少量的水,故硫酸分子不能完全电离,但是硫酸属于强电解质,故B错误;
C、氯气为单质,所以既不是电解质,也不是非电解质;氨气的水溶液导电,导电的离子是一水合氨电离的,不是氨气本身电离的,所以氨气为非电解质,故C错误;
D、三氧化硫溶于水生成硫酸,溶液和是硫酸导电,故三氧化硫是非电解质,故D正确,
故选D.
点评:本题考查了电解质与非电解质、强电解质与弱电解质的判断、溶液导电性强弱判断,题目难度中等,注意明确电解质与非电解质、强电解质与弱电解质的概念及根本区别,明确影响溶液导电性的根本因素、导电性与强弱电解质没有必然关系.

练习册系列答案
相关题目
工业制硫酸中的一步重要反应是SO2在400~500℃下的催化氧化:2SO2+O2
2SO3,这是一个正反应放热的可逆反应.如果反应在密闭容器中进行,下述有关说法中错误的是( )
| V2O5 |
| △ |
| A、使用催化剂是为了加快反应速率,提高生产效率 |
| B、在上述条件下,SO2不可能100%地转化为SO3 |
| C、为了提高SO2的转化率,应适当提高O2的浓度 |
| D、达到平衡时,SO2的浓度与SO3的浓度相等 |
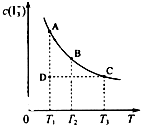 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq),某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法不正确的是( )
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq),某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法不正确的是( )| A、反应 I2(aq)+I-(aq)?I3-(aq) 的△H<0 |
| B、若反应进行到状态D时,一定有v正>v逆 |
| C、状态A与状态B相比,状态A的c(I2)大 |
| D、若温度为T1,T2反应的平衡常数分别为K1、K2,则K1>K2 |
下列说法错误的是( )
| A、由电能转化为化学能的装置叫电解池 |
| B、在电解池中跟直流电源的正极相连的电极是电解池的阳极 |
| C、在电解池中通电时,电子从电解池的阴极流出,并沿导线流回电源的负极 |
| D、电解池中阴极发生还原反应,阳极发生氧化反应 |
下列各组气体中,在通常情况下既能用浓硫酸又能用碱石灰干燥的有( )
| A、SO2、O2、N2 |
| B、HCl、Cl2、CO2 |
| C、CH4、H2、CO |
| D、SO2、Cl2、O2 |
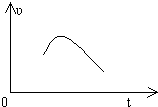 把镁条投入到盛有盐酸的敞口容器中,产生H2的速率可由如图表示,在下列因素中,①盐酸的浓度,②镁条的表面积,③溶液的温度,④氯离子的浓度,影响反应速率的因素是( )
把镁条投入到盛有盐酸的敞口容器中,产生H2的速率可由如图表示,在下列因素中,①盐酸的浓度,②镁条的表面积,③溶液的温度,④氯离子的浓度,影响反应速率的因素是( )