题目内容
18.在一定温度下将amol PCl5充入一密闭容器中达到如下平衡:PCl5(g)?PCl3(g)+Cl2(g),此时压强为P1;再向容器中通入amol PCl5,在同温下又达到平衡时的压强为P2,则下列说法中正确的是( )| A. | 2P1>P2 | B. | 2P1=P2 | C. | 2P1<P2 | D. | P1>P2 |
分析 容积固定,达平衡后再向容器中充入amol PCl5,相当于增大了压强,加入了五氯化磷,压强增大,平衡逆向移动,所以平衡时总物质的量小于原来的2倍,则平衡时压强小于原来的2倍;
解答 解:容器容积不变,加入了五氯化磷,相当于将两个相同条件下得到平衡状态的且容积不变的容器合并为一个容器,混合气体的压强增大,平衡会向左移动,所以平衡时总物质的量小于原来的2倍,相同条件下气体物质的量之比等于气体压强之比,则平衡时压强小于原来的2倍;所以2P1>P2,故A正确,
故选A.
点评 本题考查压强对化学平衡的影响,注意容器容积不变,气体物质的量增大压强增大,本题难度中等.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
8.亚硝酸钠(NaNO2)是一种工业盐,实验室可用如下装置(略去部分夹持仪器)制备.
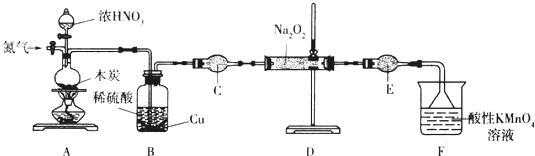
已知:①2NO+Na2O2═2NaNO2;
②3NaNO2+3HCl═3NaCl+HNO3+2NO↑+H2O;
③酸性条件下,NO和NO2都能与MnO4-反应生成NO3-和Mn2+;Na2O2能使酸性高锰酸钾溶液褪色.
(1)加热装置A前,先通一段时间N2,目的是排出装置中的空气.
(2)装置A中发生反应的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.实验结束后,将B瓶中的溶液经蒸发浓缩、冷却结晶(填操作名称)、过滤可获得CuSO4•5H2O.
(3)仪器C的名称为干燥管,其中盛放的药品为碱石灰(填名称).
(4)充分反应后,检验装置D中产物的方法是:取产物少许置于试管中,加入稀硫酸溶液中有气泡产生且在试管口上方出现红棕色气体,则产物是NaNO2(注明试剂、现象).
(5)为测定亚硝酸钠的含量,称取4.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol•L-1酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
①第一组实验数据出现异常,造成这种异常的原因可能是ac(填代号).
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶洗净后未干燥
c.滴定终点时仰视读数
②根据表中数据,计算所得固体中亚硝酸钠的质量分数86.25%.
(6)设计合理实验比较0.1mol•L-1NaNO2溶液中NO2-的水解程度和0.1mol•L-1HNO2溶液中HNO2的电离程度相对大小.(简要说明实验步骤、现象和结论,仪器和药品自选)25°C将0.1mol/LHNO2和0.1mol/LNaNO2溶液等体积混合,若测定溶液PH<7,说明HNO2的电离程度大于NO2-离子的水解程度,若测定溶液pH>7,说明NO2-离子水解程度大于HNO2的电离程度.

已知:①2NO+Na2O2═2NaNO2;
②3NaNO2+3HCl═3NaCl+HNO3+2NO↑+H2O;
③酸性条件下,NO和NO2都能与MnO4-反应生成NO3-和Mn2+;Na2O2能使酸性高锰酸钾溶液褪色.
(1)加热装置A前,先通一段时间N2,目的是排出装置中的空气.
(2)装置A中发生反应的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.实验结束后,将B瓶中的溶液经蒸发浓缩、冷却结晶(填操作名称)、过滤可获得CuSO4•5H2O.
(3)仪器C的名称为干燥管,其中盛放的药品为碱石灰(填名称).
(4)充分反应后,检验装置D中产物的方法是:取产物少许置于试管中,加入稀硫酸溶液中有气泡产生且在试管口上方出现红棕色气体,则产物是NaNO2(注明试剂、现象).
(5)为测定亚硝酸钠的含量,称取4.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol•L-1酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| KmnO4溶液体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶洗净后未干燥
c.滴定终点时仰视读数
②根据表中数据,计算所得固体中亚硝酸钠的质量分数86.25%.
(6)设计合理实验比较0.1mol•L-1NaNO2溶液中NO2-的水解程度和0.1mol•L-1HNO2溶液中HNO2的电离程度相对大小.(简要说明实验步骤、现象和结论,仪器和药品自选)25°C将0.1mol/LHNO2和0.1mol/LNaNO2溶液等体积混合,若测定溶液PH<7,说明HNO2的电离程度大于NO2-离子的水解程度,若测定溶液pH>7,说明NO2-离子水解程度大于HNO2的电离程度.
6.下列物质中属于离子化合物的是( )
| A. | H2 | B. | CH3COOH | C. | HCl | D. | (NH4)2SO4 |
13.工业上制取金刚砂的化学方程式如下:SiO2+3C=SiC+2CO↑.在这个氧化还原反应中,氧化剂和还原剂的物质的量之比为( )
| A. | 1:2 | B. | 2:1 | C. | 5:3 | D. | 3:5 |
7.用48g乙醇(其中的氧用18O标记)在浓硫酸存在条件下与足量的乙酸充分反应.下列有关叙述中不正确的是( )
| A. | 生成的水分子中含有18O | B. | 生成的乙酸乙酯中含有18O | ||
| C. | 可能生成88g乙酸乙酯 | D. | 不可能生成90g乙酸乙酯 |
8.下列有关物质应用的说法中,不正确的是( )
| A. | 工业上可用Cl2制造漂白粉 | B. | MgO 常用作耐高温材料 | ||
| C. | NaCl用于金属钠的冶炼 | D. | Na2CO3是发酵粉的主要成分之一 |
 二甲醚(CH3OCH3)被称为21世界的新型燃料,在未来可能替代汽油、液化气、煤气等并具有优良的环保性能.工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
二甲醚(CH3OCH3)被称为21世界的新型燃料,在未来可能替代汽油、液化气、煤气等并具有优良的环保性能.工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应: