题目内容
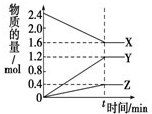
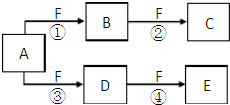 X、Y、Z是三种短周期元素,X和Z的质子数之和与Y的质子数相等,Z的电子层数是X的电子层数的2倍.A、B、C、D、E、F是中学化学中的常见物质,它们由上述三种元素中的一种、两种或三种组成,其中A是能使湿润红色石蕊试纸变蓝的气体,D、E是两种酸,F是一种单质,反应③④均在微生物作用下进行,其转化关系如图所示.
X、Y、Z是三种短周期元素,X和Z的质子数之和与Y的质子数相等,Z的电子层数是X的电子层数的2倍.A、B、C、D、E、F是中学化学中的常见物质,它们由上述三种元素中的一种、两种或三种组成,其中A是能使湿润红色石蕊试纸变蓝的气体,D、E是两种酸,F是一种单质,反应③④均在微生物作用下进行,其转化关系如图所示.回答下列问题:
(1)A的电子式为
(2)A和E反应生成G,C与G中都含有
(3)反应③中如果转移的电子为3mol,则被氧化的A为
(4)科学家发明了使ZX3直接用于燃料电池的方法,其装置用铂作电极,加入碱性电解质溶液,往一极通入空气,另一电极通入ZX3并使之转化为无污染的气体,试写出负极的电极反应式:
(5)由Z、X两元素形成的含10个电子的阳离子可和XSO4-形成一种盐A,若往A的溶液中缓缓滴入稀NaOH溶液至溶液恰好呈中性,则溶液中所含离子浓度由大到小的顺序为:
考点:无机物的推断
专题:推断题
分析:A、B、C、D、E、F是中学化学中的常见物质,它们由上述三种元素中的一种、两种或三种组成,其中A是能使湿润红色石蕊试纸变蓝的气体,则A是NH3,氨气能连续和F单质反应,氨气能连续被氧化,则F是O2,
X、Y、Z是三种短周期元素,X和Z的质子数之和与Y的质子数相等,Z的电子层数是X的电子层数的2倍,则X是H元素、Z是N元素、Y是O元素,
D、E是两种酸,F是一种单质,反应③④均在微生物作用下进行,D为HNO2,E为HNO3,氨气被氧气氧化生成NO,则B是NO,NO被氧气氧化生成NO2,则C是NO2,再结合题目分析解答.
X、Y、Z是三种短周期元素,X和Z的质子数之和与Y的质子数相等,Z的电子层数是X的电子层数的2倍,则X是H元素、Z是N元素、Y是O元素,
D、E是两种酸,F是一种单质,反应③④均在微生物作用下进行,D为HNO2,E为HNO3,氨气被氧气氧化生成NO,则B是NO,NO被氧气氧化生成NO2,则C是NO2,再结合题目分析解答.
解答:
解:A、B、C、D、E、F是中学化学中的常见物质,它们由上述三种元素中的一种、两种或三种组成,其中A是能使湿润红色石蕊试纸变蓝的气体,则A是NH3,氨气能连续和F单质反应,氨气能连续被氧化,则F是O2,
X、Y、Z是三种短周期元素,X和Z的质子数之和与Y的质子数相等,Z的电子层数是X的电子层数的2倍,则X是H元素、Z是N元素、Y是O元素,
D、E是两种酸,F是一种单质,反应③④均在微生物作用下进行,D为HNO2,E为HNO3,氨气被氧气氧化生成NO,则B是NO,NO被氧气氧化生成NO2,则C是NO2,
(1)通过以上分析知,A是氨气,氨气中N原子和每个H原子之间都存在一个共价键,其电子式为 ,故答案为:
,故答案为: ;
;
(2)A是氨气、E是硝酸,二者反应生成G,G为NH4NO3,C是NO2,C和G都含有极性共价键,故答案为:共价键(或极性共价键);
(3)氨气和氧气再微生物作用下生成亚硝酸,反应的化学方程式为:2NH3+3O2
2HNO2+2H2O,该反应中转移电子的物质的量=3mol×4=12mol,反应③中如果转移的电子为3mol,则被氧化的A的物质的量=
×2=0.5mol,故答案为:0.5;
(4)氨气碱性燃料电池中,负极上氨气失电子发生氧化反应生成氮气和水,正极上氧气得电子和水反应生成氢氧根离子,所以负极电极反应式为2NH3-6e-+6OH-=N2+6H2O,正极电极反应式为O2+2H2O+4e-=4OH-,故答案为:2NH3-6e-+6OH-=N2+6H2O;
(5)Z、X两元素形成的含10个电子的阳离子是NH4+,可和HSO4-形成一种盐A,A为NH4HSO4,若往A的溶液中缓缓滴入稀NaOH溶液至溶液恰好呈中性,溶液中的溶质是Na2SO4、NH3.H2O、(NH4)2SO4,溶液呈中性,则c(H+)=c(OH-),根据电荷守恒得c(Na+)+c(NH4+)=2c(SO42-),如果硫酸氢铵和NaOH以1:1反应,则溶液呈酸性,要使溶液呈中性,则氢氧化钠应该稍微过量,所以根据物料守恒得c(Na+)>c(SO42-)>c(NH4+),则溶液中所含离子浓度由大到小的顺序为:c(Na+)>c(SO42-)>c(NH4+)>c(H+)=c(OH-),故答案为:c(Na+)>c(SO42-)>c(NH4+)>c(H+)=c(OH-).
X、Y、Z是三种短周期元素,X和Z的质子数之和与Y的质子数相等,Z的电子层数是X的电子层数的2倍,则X是H元素、Z是N元素、Y是O元素,
D、E是两种酸,F是一种单质,反应③④均在微生物作用下进行,D为HNO2,E为HNO3,氨气被氧气氧化生成NO,则B是NO,NO被氧气氧化生成NO2,则C是NO2,
(1)通过以上分析知,A是氨气,氨气中N原子和每个H原子之间都存在一个共价键,其电子式为
 ,故答案为:
,故答案为: ;
;(2)A是氨气、E是硝酸,二者反应生成G,G为NH4NO3,C是NO2,C和G都含有极性共价键,故答案为:共价键(或极性共价键);
(3)氨气和氧气再微生物作用下生成亚硝酸,反应的化学方程式为:2NH3+3O2
| ||
| 3mol |
| 12mol |
(4)氨气碱性燃料电池中,负极上氨气失电子发生氧化反应生成氮气和水,正极上氧气得电子和水反应生成氢氧根离子,所以负极电极反应式为2NH3-6e-+6OH-=N2+6H2O,正极电极反应式为O2+2H2O+4e-=4OH-,故答案为:2NH3-6e-+6OH-=N2+6H2O;
(5)Z、X两元素形成的含10个电子的阳离子是NH4+,可和HSO4-形成一种盐A,A为NH4HSO4,若往A的溶液中缓缓滴入稀NaOH溶液至溶液恰好呈中性,溶液中的溶质是Na2SO4、NH3.H2O、(NH4)2SO4,溶液呈中性,则c(H+)=c(OH-),根据电荷守恒得c(Na+)+c(NH4+)=2c(SO42-),如果硫酸氢铵和NaOH以1:1反应,则溶液呈酸性,要使溶液呈中性,则氢氧化钠应该稍微过量,所以根据物料守恒得c(Na+)>c(SO42-)>c(NH4+),则溶液中所含离子浓度由大到小的顺序为:c(Na+)>c(SO42-)>c(NH4+)>c(H+)=c(OH-),故答案为:c(Na+)>c(SO42-)>c(NH4+)>c(H+)=c(OH-).
点评:本题考查了无机物推断,涉及物质推断、离子浓度大小比较、原电池原理、氧化还原反应等知识点,根据物质的性质结合反应条件推断物质,再结合物质的性质、原电池原理、氧化还原反应实质等知识点来分析解答即可,难点是(5)中离子浓度大小比较,题目难度中等.

练习册系列答案
相关题目
下列说法正确的是( )
| A、已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ?mol-1,则H2SO4(aq)+Ba(OH)2(aq)═BaSO4(s)+2H2O(l)△H=2×(-57.3)kJ?mol-1 | ||||
| B、已知:H2(g)+F2(g)═2HF(g)△H=-270 kJ?mol-1,则1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ | ||||
C、500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)
| ||||
D、葡萄糖的燃烧热是2 800 kJ?mol-1,则
|
下列化学反应中,属于氧化还原的化合反应是( )
| A、Na2CO3+CaCl2═CaCO3↓+2NaCl | ||||
| B、Fe+CuSO4═Cu+FeSO4 | ||||
C、2NaHCO3
| ||||
| D、Na2O2+SO2═Na2SO4 |
 (1)在一个容积为2L的密闭容器中,充入1mol SO2和1mol O2,一定条件下发生反应2SO2+O2?2SO3,3分钟后测得SO3的物质的量为0.6mol,则此时O2的物质的量浓度为
(1)在一个容积为2L的密闭容器中,充入1mol SO2和1mol O2,一定条件下发生反应2SO2+O2?2SO3,3分钟后测得SO3的物质的量为0.6mol,则此时O2的物质的量浓度为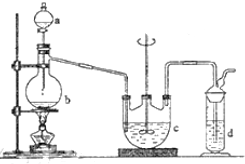 硫代硫酸钠(Na2S2O3)可用做分析试剂及鞣革还原剂.它受热、遇酸易分解.工业上可用反应:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2制得.实验室模拟该工业过程的装置如图所示.回答下列问题:
硫代硫酸钠(Na2S2O3)可用做分析试剂及鞣革还原剂.它受热、遇酸易分解.工业上可用反应:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2制得.实验室模拟该工业过程的装置如图所示.回答下列问题: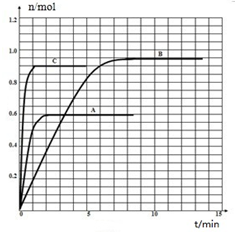
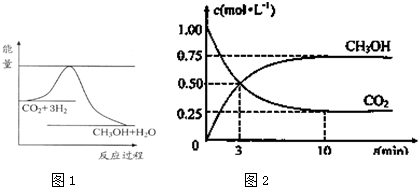
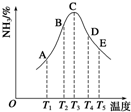 在容积相同的密闭容器内,分别充入同量的N2和H2,在不同温度下,任其发生反应N2(g)+3H2(g)?2NH3(g),并分别在t秒时测定其中NH3的体积分数,如图:
在容积相同的密闭容器内,分别充入同量的N2和H2,在不同温度下,任其发生反应N2(g)+3H2(g)?2NH3(g),并分别在t秒时测定其中NH3的体积分数,如图: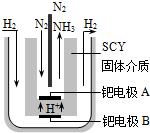 合成氨对工农业发展有着重要意义,下面是对有关其应用的研究.
合成氨对工农业发展有着重要意义,下面是对有关其应用的研究.