题目内容
下列说法中正确的是( )
| A、只含有非金属元素的化合物可能是离子化合物 |
| B、第ⅠA族元素都比第ⅡA族元素金属性强 |
| C、只含有共价键的物质一定是共价化合物 |
| D、同主族元素原子半径越小越容易失去电子 |
考点:离子化合物的结构特征与性质,元素周期律的作用,共价键的形成及共价键的主要类型
专题:元素周期律与元素周期表专题,化学键与晶体结构
分析:A.只含有非金属元素的化合物,可能为共价化合物,也可能为离子化合物;
B.Ca的金属性比Na强;
C.只含有共价键的物质,可能为单质;
D.同主族元素原子半径越小,金属性越弱.
B.Ca的金属性比Na强;
C.只含有共价键的物质,可能为单质;
D.同主族元素原子半径越小,金属性越弱.
解答:
解:A.只含有非金属元素的化合物,可能为共价化合物如HCl,也可能为离子化合物如铵盐,故A正确;
B.Ca的金属性比Na强,则应为同周期第ⅠA族元素都比第ⅡA族元素金属性强,故B错误;
C.只含有共价键的物质,可能为单质,如氢气、氮气等,故C错误;
D.同主族元素原子半径越小,金属性越弱,则越难失去电子,故D错误;
故选A.
B.Ca的金属性比Na强,则应为同周期第ⅠA族元素都比第ⅡA族元素金属性强,故B错误;
C.只含有共价键的物质,可能为单质,如氢气、氮气等,故C错误;
D.同主族元素原子半径越小,金属性越弱,则越难失去电子,故D错误;
故选A.
点评:本题考查较综合,涉及离子化合物及化学键、元素周期律等,为高频考点,把握物质中的化学键形成及特殊物质中的化学键为解答的关键,注意利用实例分析解答,题目难度不大.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
 对于锌、铜和稀硫酸组成的原电池(如图),下列有关说法正确的是( )
对于锌、铜和稀硫酸组成的原电池(如图),下列有关说法正确的是( )①Zn是负极
②电子由Zn经外电路流向Cu
③Zn极发生氧化反应生成Zn2+
④H+在溶液中由Cu极向Zn极迁移.
| A、①②④ | B、②③④ |
| C、①②③ | D、①②③④ |
有关下列四个装置的描述正确的是( )
A、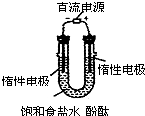 工作时溶液中OH-向阳极移动,因此阳极附近溶液先变红色 |
B、 装置中Zn作正极,Cu作负极 |
C、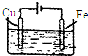 可实现对铁制品表面镀铜 |
D、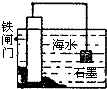 可实现对铁闸门保护 |
下列除去杂质的方法正确的是( )
| A、除去CO2中混有的CO:用澄清石灰水洗气 |
| B、除去FeCl2溶液中混有的FeCl3:加入过量铁粉,过滤 |
| C、除去BaCO3固体中混有的BaSO4:加过量盐酸后,过滤、洗涤 |
| D、除去Cu粉中混有的CuO:加适量稀硝酸后,过滤、洗涤 |
下列有关金属元素特征的叙述正确的是( )
| A、金属元素的原子只有还原性,其阳离子只有氧化性 |
| B、在化学反应中,由于铝原子能失去三个电子,而钠原子只能失去一个电子,所以铝的还原性比钠强 |
| C、钠元素在自然界中以化合态存在 |
| D、金属元素的单质在常温下都为固体 |
分类是学习化学的重要方法.下列归纳正确的是( )
| A、SO2、SiO2、CO均为酸性氧化物 |
| B、纯碱、烧碱、熟石灰都属于碱类 |
| C、氨气、冰醋酸、食盐均为电解质 |
| D、冰和干冰既是纯净物又是化合物 |
下列说法不正确的是( )
| A、淀粉、蛋白质、橡胶都是高分子化合物,但不一定是天然高分子化合物 |
| B、能与氢气发生加成反应的烃中一定含有碳碳双键 |
| C、煤的干馏、石油催化重整、石油裂化都生成了新物质,都属于化学变化 |
| D、汽油不一定能使溴的四氯化碳溶液褪色 |
水的相对分子质量为18,则一个水分子的质量为( )
A、
| ||
B、
| ||
| C、18NA g | ||
D、
|
