题目内容
下列可用来鉴别SO2和CO2气体的试剂有( )
①澄清石灰水②氢硫酸③氯水④酸性高锰酸钾⑤硝酸钡溶液⑥紫色石蕊试液⑦品红溶液.
①澄清石灰水②氢硫酸③氯水④酸性高锰酸钾⑤硝酸钡溶液⑥紫色石蕊试液⑦品红溶液.
| A、②③④⑤⑦ |
| B、①④⑤⑥⑦ |
| C、①②③⑥⑦ |
| D、②③④⑥⑦ |
考点:物质的检验和鉴别的基本方法选择及应用
专题:
分析:SO2和CO2均为酸性氧化物,二氧化硫具有还原性,具有漂白性,结合物质的性质差异来解答.
解答:
解:①均使澄清石灰水变浑浊,现象相同,不能鉴别,故不选;
②二氧化硫与氢硫酸反应生成淡黄色沉淀,二氧化碳不能,可鉴别,故选;
③二氧化硫与氯水反应生成无色溶液,而二氧化碳不能,可鉴别,故选;
④二氧化硫使酸性高锰酸钾褪色,二氧化碳不能,可鉴别,故选;
⑤二氧化硫与硝酸钡溶液发生氧化还原反应生成硫酸钡沉淀,二氧化碳不能,可鉴别,故选;
⑥均使紫色石蕊试液变红,现象相同,不能鉴别,故不选;
⑦二氧化硫使品红溶液褪色,二氧化碳不能,可鉴别,故选;
故选A.
②二氧化硫与氢硫酸反应生成淡黄色沉淀,二氧化碳不能,可鉴别,故选;
③二氧化硫与氯水反应生成无色溶液,而二氧化碳不能,可鉴别,故选;
④二氧化硫使酸性高锰酸钾褪色,二氧化碳不能,可鉴别,故选;
⑤二氧化硫与硝酸钡溶液发生氧化还原反应生成硫酸钡沉淀,二氧化碳不能,可鉴别,故选;
⑥均使紫色石蕊试液变红,现象相同,不能鉴别,故不选;
⑦二氧化硫使品红溶液褪色,二氧化碳不能,可鉴别,故选;
故选A.
点评:本题考查物质的鉴别,为高频考点,把握物质的性质和性质差异、发生的反应和现象为解答的关键,注意现象相同不能鉴别物质,题目难度不大.

练习册系列答案
相关题目
部分弱酸的电离平衡常数如下表:下列说法正确的是( )
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | K=1.77×10-4 | K=4.9×10-10 | K1=4.2×10-7 K2=5.6×10-11 |
| A、0.1mol?L-1NaHCO3溶液中浓度的大小:c(Na+)>c(HCO 3-)>c(H+)>c(OH-) |
| B、少量的CO2通入到NaCN溶液中 CN-+H2O+CO2=HCN+HCO 3- |
| C、用0.1mol?L-1NaOH溶液中和等浓度的HCN和HCOOH时前者所需NaOH溶液体积大 |
| D、0.1mol?L-1HCOONa溶液比0.1mol?L-1NaCN溶液所含离子总数小 |
一水合氨是一种常见的弱碱,为了证明一水合氨是弱电解质.,某同学开展了题为“一水合氨是弱电解质的实验研究”的探究活动.该同学设计了如下方案,其中错误的是( )
| A、先配制一定量的0.10mol?L-1氨水,然后测溶液的pH,若pH小于13,则可证明一水合氨为弱电解质. |
| B、先分别配制一定量0.01mol?L-1氨水和0.10mol?L-1氨水,分别用pH计测它们的pH,若两者的pH相差小于1个单位,则可证明一水合氨是弱电解质. |
| C、先测0.10mol?L-1 氨水的pH,然后将其加热至100℃,再测pH,如果pH变大则可证明一水合氨是弱电解质. |
| D、配制一定量的NH4Cl溶液.测pH.若常温下pH小于7.则证明一水合氨是弱电解质. |
利用下列实验装置能完成相应实验的是( )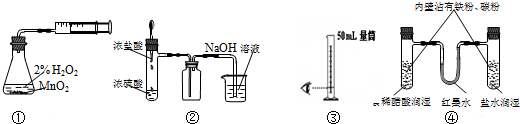

| A、装置①测定化学反应速率 |
| B、装置②制取并吸收HCl |
| C、装置③量取8.5mL的稀硫酸 |
| D、装置④模拟铁的腐蚀 |
下列关于碱金属及其化合物的叙述错误的是( )
| A、金属钠投入Ca(HCO3)2溶液,反应后有白色沉淀析出 |
| B、干粉灭火器能用于扑灭金属钠、钾的着火 |
| C、生理盐水的质量分数为0.9%,与人体的血液中含量相同,它的溶质是NaCl |
| D、取用金属钠、钾时,所需实验用品有小刀、镊子、滤纸、玻璃片 |
在某无色、透明的强酸性溶液中,能大量共存的离子组是( )
| A、NH4+、NO3-、Al3+、Cl- |
| B、Na+、SO42-、Ba2+、NO3- |
| C、MnO4-、K+、SO42-、Na+ |
| D、H+、SO42-、HCO3-、Na+ |