题目内容
下列有关溶液中微粒浓度关系的叙述正确的是
A.0.1 mol·L-1NH4Cl溶液中:c(NH4+)>c(Cl-)>c(H+)>c(OH-)
B.溶有等物质的量NaClO、NaHCO3的溶液中:c(HClO)+c(ClO-)=c(HCO3—)+c(H2CO3)+c(CO32—)
C.pH=5.6的CH3COOH与CH3COONa混合溶液中:c(Na+)<c(CH3COO-)
D.25℃时,pH=7的NH4Cl与NH3·H2O混合溶液:c(H+)= c(OH-)=c(NH4+)=c(Cl-)
BC
【解析】
试题分析:A、0.1 mol·L-1NH4Cl溶液中NH4+水解,溶液呈酸性:c(Cl-)>c(NH4+)> c(H+)>c(OH-),错误;B、根据物料守恒得c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-)=1/2c(Na+),正确;C、根据电荷守恒判断,c(H+)+ c(Na+)= c(CH3COO-)+ c(OH-),溶液呈酸性,c(OH-)<c(H+),所以c(Na+)<c(Cl-),正确;D、25℃时,pH=7的NH4Cl与NH3·H2O混合溶液:c(H+)= c(OH-)<c(NH4+)=c(Cl-),错误。
考点:考查离子浓度大小比较。

练习册系列答案
相关题目
下列叙述I和II均正确并有因果关系的是
选项 | 叙述I | 叙述II |
A | 实验室常用Al2(SO4)3溶液与氨水溶液制备Al(OH)3沉淀 | Al(OH)3不溶于碱 |
B | NaHCO3为强碱弱酸盐 | NaHCO3 -溶液显碱性 |
C | SO2具有氧化性 | SO2可用品红溶液检验 |
D | Fe(OH)3胶体有丁达尔效应 | Fe(OH)3胶体可以用FeCl3浓溶液与NaOH溶液反应制得 |

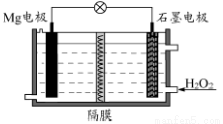
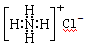
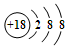
 NiOOH + MH
NiOOH + MH