题目内容
6.下列仪器是用于测定有机物的相对分子质量的是( )| A. | 元素分析仪 | B. | 质谱仪 | C. | 红外光谱仪 | D. | 核磁共振仪 |
分析 A.元素分析仪来确定有机化合物中的元素组成;
B.质谱仪能测出有机物相对分子质量;
C.用于检测有机物中特殊官能团及机构特征,主要适用于定性分析有机化合物结构;
D.核磁共振仪能测出有机物中氢原子子的种类以及数目之比.
解答 解:质谱仪能测出有机物相对分子质量,符合题意.
故选B.
点评 本题主要考查了有机物结构研究中常见仪器的作用,难度不大,掌握常见仪器的作用是解题的关键.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案
相关题目
16.化学反应总是伴随着丰富多彩的颜色的变化,下列说法错误的是( )
| A. | 将Na2O2固体投入滴加了少许酚酞的蒸馏水中,溶液先变红后褪色 | |
| B. | 用玻璃棒蘸取浓硝酸滴加到pH试纸上,试纸先变红后变成白色 | |
| C. | 向胆矾晶体(CuSO4•5H2O)滴加浓硫酸,晶体由蓝色变为黑色 | |
| D. | 将SO2通入品红溶液中,溶液颜色褪去,加热后又变成红色 |
17.下列化学实验事实及其解释或结论都正确的是( )
| A. | 用玻璃棒蘸取新制氯水,滴在pH试纸上,然后与比色卡对照,可测定新制氯水的pH | |
| B. | 向10mL 0.1 mol/L的AgNO3溶液中滴加10滴0.1 mol/L的NaCl溶液,有白色沉淀生成,再向其中滴加0.1 mol/L的KI溶液,沉淀变为黄色,说明相同温度下AgCl溶解度大于AgI的溶解度 | |
| C. | 向1 mL 1%的NaOH溶液中加入2 mL 2%的CuSO4溶液,振荡,再加入0.5 mL有机物Y,加热,未出现砖红色沉淀,说明Y中不含醛基 | |
| D. | 取少量卤代烃Y在碱性溶液中水解,用硝酸酸化至酸性,再滴加AgNO3溶液,生成淡黄色沉淀,说明卤代烃中含有溴元素 |
14.上海作为2010年世博会的举办城市,公共交通的“绿色”也已经在进行,以二甲醚(简称甲醚)为燃料的公交车作为“绿色”花园中的一点鲜艳的绿色已经正式“登台”.下列叙述正确的是( )
| A. | 甲醚作燃料会产生氮的氧化物和碳氢化合物等污染物 | |
| B. | 甲醚可由甲醇在一定条件下发生消去反应而制得 | |
| C. | 甲醚与乙醇是同分异构体 | |
| D. | 1 mol甲醚完全燃烧消耗的氧气与1 mol甲醇完全燃烧消耗的氧气相同 |
1.14C是碳的一种同位素,NA为阿伏加德罗常数,下列说法不正确的是( )
| A. | 1mol14CH4分子中所含中子数为8NA | |
| B. | 7g14C原子形成的石墨中所含质子数为3NA | |
| C. | 17g甲基(-14CH3)所含电子数为8NA | |
| D. | 标准状况下22.4L14CO2的分子数为NA |
11.苹果酸的结构简式为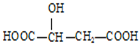 ,下列说法正确的是( )
,下列说法正确的是( )
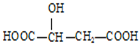 ,下列说法正确的是( )
,下列说法正确的是( )| A. | HOOC-CH2-CH(OH)-COOH与苹果酸互为同分异构体 | |
| B. | 1mol苹果酸可与3mol NaOH发生中和反应 | |
| C. | 1mol苹果酸与足量金属Na反应生成生成1mol H2 | |
| D. | 苹果酸中能发生酯化反应的官能团有2种 |
18.下列关于SiO2和CO2的说法中不正确的是( )
| A. | CO2和SiO2都能与碱及碱性氧化物反应 | |
| B. | CO2和SiO2都能与水反应生成相应的酸 | |
| C. | CO2和SiO2都能与焦炭反应生成CO | |
| D. | SiO2可用于制光导纤维,干冰可用于人工降雨 |
15.下列说法正确的是( )
| A. | 阴阳离子间通过静电吸引形成的化学键叫做离子键 | |
| B. | HF,HCl,HBr,HI的热稳定性和酸性均依次减弱 | |
| C. | 元素非金属越强,其对应含氧酸的酸性就越强 | |
| D. | 元素周期律是元素原子核电子排布周期性变化的结果 |
16.已知X、Y、Z都是短周期元素,它们的原子序数依次递增,X原子的电子层数与它的核外电子总数相等,而Z原子的最外层电子数是次外层的3倍,Y和Z可以形成两种以上气态化合物,则下列说法错误的是( )
| A. | Y和Z可以组成一种Y和Z的质量比为7:20的化合物 | |
| B. | X、Y、Z组成的一种离子化合物,其中X、Y、Z元素原子个数比可能为4:2:3 | |
| C. | X和Z可以形成X2Z和X2Z2型化合物,所含共价键类型不完全相同 | |
| D. | 由X、Y、Z三种元素中的任意两种组成的具有10电子的微粒有2种 |