题目内容
与1.8g H2O含有相同氧原子数的H2SO4的质量为( )
| A、0.1 g |
| B、0.2 g |
| C、2.45 g |
| D、4.9 g |
考点:物质的量的相关计算
专题:计算题
分析:根据质量和微粒数公式m=nM=
M,列等式来计算即可.
| N |
| NA |
解答:
解:1.8g水的物质的量为
=0.1mol,即含有0.1mol氧原子,
和
=0.025mol的硫酸含有相同的氧原子,0.025mol硫酸的质量为m=nM=0.025mol×98g/mol=2.45g.
故选C.
| 1.8g |
| 18g/mol |
和
| 0.1mol |
| 4 |
故选C.
点评:本题考查物质的量的有关计算,明确质量和微粒数之间的关系公式为m=nM=
M即可解答,难度不大.
| N |
| NA |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
设NA表示阿佛加德常数,下列叙述中正确的是( )
| A、分子数为NA的O2与CH3OH的混合物质量为32g |
| B、在0.1mol?L-1的碳酸钾溶液中,阴离子数目大于0.1NA |
| C、1.5 mol NO2与足量H2O反应,转移的电子数为1mol |
| D、32g铜与足量浓硫酸在加热条件下充分反应,生成11.2L气体 |
下列各组离子在水溶液中能大量共存的是( )
| A、Fe3+、Fe2+、Cl-、OH- |
| B、Fe2+、H+、Na+、NO3- |
| C、H+、Fe2+、SO42-、Cl- |
| D、Fe3+、NO3-、K+、I- |
ClO2和Cl2一样,可作引用水的消毒剂,且这两种消毒剂的消毒原理都可看作是与水反应生成Cl-和原子态氧,起消毒作用的是原子态氧,因为它具有强氧化性.据此计算同质量的ClO2和Cl2消毒效率之比为( )
| A、1:2 | B、5:2 |
| C、1:1 | D、2.63:1 |
下列反应的离子方程式书写正确的是( )
| A、CuSO4溶液中加入Na:2Na+Cu2+═Cu+2Na+ |
| B、金属钠溶于水:Na+H2O=Na++OH-+H2↑ |
| C、金属铝溶于盐酸中:2Al+6H+=2Al3++3H2↑ |
| D、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
下列各装置能构成原电池的是( )
A、 |
B、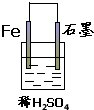 |
C、 |
D、 |
如图所示装置可用于( )


| A、加热NaHCO3制CO2 |
| B、用Cu与稀HNO3反应制NO |
| C、加热氯化铵和消石灰混合物,制取氨气 |
| D、加热氯酸钾和少量二氧化锰,制取氧气 |
现将金属镁和铝的混合物7.5g完全溶解于一定浓度足量的硝酸溶液中,收集反应产生的A气体.向所得溶液中加入过量烧碱溶液,得到沉淀11.6g.则气体A的成分可能是( )
| A、0.2mol NO和0.1mol NO2 |
| B、0.3 mol NO |
| C、0.1mol NO、0.2mol NO2和0.1mol N2O4 |
| D、0.3 mol NO2和0.1mol N2O4 |