题目内容
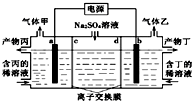 电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法正确的是( )
电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法正确的是( )| A、a极与电源的负极相连 |
| B、产物丙为硫酸溶液 |
| C、离子交换膜d为阳离子交换膜(允许阳离子通过) |
| D、a电极反应式为2H2O+2e-═2OH-+H2↑ |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:装置图分析可知是电解装置,电极硫酸钠溶液,实质实质是电解水,气体甲与气体乙的体积比约为1:2,气体甲为氧气,气体乙为氢气,阳极生成氧气,电极反应4OH--4e-=2H2O+O2,阴极生成氢气,2H++2e-=H2↑,气体体积比为1:2,所以判断a电极是阳极,b电极是阴极,在阳极室得到硫酸,在阴极室得到氢氧化钠,则c为阴离子交换膜,d为阳离子交换膜.
解答:
解:装置图分析可知是电解装置,电极硫酸钠溶液,实质实质是电解水,气体甲与气体乙的体积比约为1:2,气体甲为氧气,气体乙为氢气,阳极生成氧气,电极反应4OH--4e-=2H2O+O2,阴极生成氢气,2H++2e-=H2↑,气体体积比为1:2,所以判断a电极是阳极,b电极是阴极,在阳极室得到硫酸,在阴极室得到氢氧化钠,则c为阴离子交换膜,d为阳离子交换膜;
A、分析可知a电极为阳极,与电源正极相连,故A错误;
B、阳极a生成氧气,电极反应4OH--4e-=2H2O+O2↑,阳极室水的 电离平衡被破坏生成氢离子,生成产物丙为硫酸,阴极生成氢气,2H++2e-=H2↑,生成产物丁为氢氧化钠,故B正确;
C、阳极a生成氧气,电极反应4OH--4e-=2H2O+O2↑,阳极室水的 电离平衡被破坏生成氢离子,生成产物丙为硫酸,阴极生成氢气,2H++2e-=H2↑,生成产物丁为氢氧化钠,则c为阴离子交换膜,d为阳离子交换膜,故C正确;
D、阳极a生成氧气,电极反应4OH--4e-=2H2O+O2↑,故D错误;
故选BC.
A、分析可知a电极为阳极,与电源正极相连,故A错误;
B、阳极a生成氧气,电极反应4OH--4e-=2H2O+O2↑,阳极室水的 电离平衡被破坏生成氢离子,生成产物丙为硫酸,阴极生成氢气,2H++2e-=H2↑,生成产物丁为氢氧化钠,故B正确;
C、阳极a生成氧气,电极反应4OH--4e-=2H2O+O2↑,阳极室水的 电离平衡被破坏生成氢离子,生成产物丙为硫酸,阴极生成氢气,2H++2e-=H2↑,生成产物丁为氢氧化钠,则c为阴离子交换膜,d为阳离子交换膜,故C正确;
D、阳极a生成氧气,电极反应4OH--4e-=2H2O+O2↑,故D错误;
故选BC.
点评:本题考查了电解原理的分析应用,电极产物和电极名称判断是解题关键,题目难度中等,侧重于考查学生对电解知识的综合应用能力.

练习册系列答案
相关题目
相同物质的量的镁和铝分别与足量的稀盐酸反应,生成氢气的质量之比为( )
| A、1:1 | B、2:3 |
| C、3:4 | D、2:1 |
下列实验方法或操作:
①用100mL筒量配制60mL10% 的盐酸;②称量没有腐蚀性固体药品时,把药品放在托盘上称量;③浓硫酸沾到皮肤上要先用抹布擦再用大量水冲洗;④用托盘天平称取5.20gNaCl晶体;⑤蒸馏开始时应先加热在开冷凝水;⑥萃取操作时选择的萃取剂的密度不必比水大;⑦用容量瓶配制一定浓度的某溶液后,将溶液保存在容量瓶中并贴上标签.其中正确的是( )
①用100mL筒量配制60mL10% 的盐酸;②称量没有腐蚀性固体药品时,把药品放在托盘上称量;③浓硫酸沾到皮肤上要先用抹布擦再用大量水冲洗;④用托盘天平称取5.20gNaCl晶体;⑤蒸馏开始时应先加热在开冷凝水;⑥萃取操作时选择的萃取剂的密度不必比水大;⑦用容量瓶配制一定浓度的某溶液后,将溶液保存在容量瓶中并贴上标签.其中正确的是( )
| A、③⑥ | B、②③⑦ |
| C、①③⑥ | D、③⑤⑥ |
从海带中提取碘用到过滤、萃取操作,进行这两项操作时不需要的仪器是( )
| A、烧杯 | B、烧瓶 |
| C、玻璃棒 | D、分液漏斗 |
工业上常用焦炭和二氧化硅在电炉中发生反应制取粗硅,化学方程式;SiO2+2C
Si+2CO.下列说法不正确的是( )
| ||
| A、该反应属于置换反应 |
| B、C是还原剂,发生还原反应 |
| C、SiO2是氧化剂,在反应中还原 |
| D、氧化还原反应的实质是电子的转移 |
下列关于钠的叙述中不正确的是( )
| A、钠具有很强的还原性 |
| B、钠原子的最外层只有一个电子 |
| C、在实验室中,钠通常保存在石蜡油或煤油中 |
| D、钠在常温下不易被氧化 |
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
| A、HClO的结构式:H-Cl-O | ||
B、Na2O2的电子式: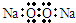 | ||
C、中子数为20的氯原子:
| ||
D、铝原子的结构示意图 |
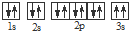 ,违背了
,违背了