题目内容
用18mol/L的浓硫酸配制80mL、1.0mol/L的硫酸.
(1)所用容量瓶的规格为 mL,所用浓硫酸的体积为 mL.
(2)若实验仪器有:
A、100mL量筒 B、选定规格的容量瓶 C、玻璃棒 D、10mL量筒 E、胶头滴管 F、50mL烧杯
实验时选用仪器的先后顺序是(填编号)
(3)第一次将烧杯中的溶液移入容量瓶后,玻璃棒应放在 (填序号)
A、原稀释所用烧杯中. B、桌面上.
C、干净的纸上. D、蒸馏水中洗净以备再用.
(4)移液前容量瓶有少量蒸馏水则所配溶液的浓度 (填序号)
A、偏高 B、偏低 C、不变
(5)定容时俯视刻度线,则所配溶液的浓度 (填序号)
A、偏高 B、偏低 C、不变.
(1)所用容量瓶的规格为
(2)若实验仪器有:
A、100mL量筒 B、选定规格的容量瓶 C、玻璃棒 D、10mL量筒 E、胶头滴管 F、50mL烧杯
实验时选用仪器的先后顺序是(填编号)
(3)第一次将烧杯中的溶液移入容量瓶后,玻璃棒应放在
A、原稀释所用烧杯中. B、桌面上.
C、干净的纸上. D、蒸馏水中洗净以备再用.
(4)移液前容量瓶有少量蒸馏水则所配溶液的浓度
A、偏高 B、偏低 C、不变
(5)定容时俯视刻度线,则所配溶液的浓度
A、偏高 B、偏低 C、不变.
考点:溶液的配制
专题:实验题
分析:(1)根据浓硫酸稀释前后,溶质的物质的量不变来计算需要浓硫酸的体积,依据配置溶液的体积确定容量瓶的规格;
(2)依据配置一定物质的量浓度溶液的一般步骤解答;
(3)玻璃棒引流时沾有溶质,为保证溶质全部转移到容量瓶,应放在稀释用的烧杯中;
(4)(5)根据c=
分析操作对溶质的物质的量或对溶液的体积的影响判断.
(2)依据配置一定物质的量浓度溶液的一般步骤解答;
(3)玻璃棒引流时沾有溶质,为保证溶质全部转移到容量瓶,应放在稀释用的烧杯中;
(4)(5)根据c=
| n |
| V |
解答:
解:(1)要配置80mL、1.0mol/L的硫酸溶液,应选用100mL的容量瓶;
浓硫酸稀释前后,溶质的物质的量不变,设需要浓硫酸的体积为V,则V×18mol/L=100mL×1.0mol/L,解得V=5.6mL;
故答案为:100;5.6;
(2)配制100mL1.0mol/L的稀硫酸的步骤为:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀等,选用的仪器及先后顺序为:10mL量筒、50mL烧杯、玻璃棒、100mL容量瓶、胶头滴管,
故答案为:DCFBE或DFCBE;
(3)玻璃棒引流时沾有溶质,为保证溶质全部转移到容量瓶,应放在稀释用的烧杯中,
故选:A;
(4)移液前容量瓶有少量蒸馏水对溶质的物质的量和溶液的体积都不会产生影响,溶液的浓度不变;
故选:C;
(5)定容时俯视刻度线,导致溶液的体积偏小,溶液的浓度偏高;
故选:A.
浓硫酸稀释前后,溶质的物质的量不变,设需要浓硫酸的体积为V,则V×18mol/L=100mL×1.0mol/L,解得V=5.6mL;
故答案为:100;5.6;
(2)配制100mL1.0mol/L的稀硫酸的步骤为:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀等,选用的仪器及先后顺序为:10mL量筒、50mL烧杯、玻璃棒、100mL容量瓶、胶头滴管,
故答案为:DCFBE或DFCBE;
(3)玻璃棒引流时沾有溶质,为保证溶质全部转移到容量瓶,应放在稀释用的烧杯中,
故选:A;
(4)移液前容量瓶有少量蒸馏水对溶质的物质的量和溶液的体积都不会产生影响,溶液的浓度不变;
故选:C;
(5)定容时俯视刻度线,导致溶液的体积偏小,溶液的浓度偏高;
故选:A.
点评:本题考查学生配制一定物质的量浓度的溶液以及仪器的使用方面的知识,可以根据所学知识进行回答,难度不大,有利于培养学生的逻辑思维能力和严谨的规范实验操作能力.

练习册系列答案
相关题目
在一定体积pH=2的NaHSO4溶液中,逐滴加入一定物质的量浓度的Ba(OH)2溶液,当溶液中的硫酸根恰好完全沉淀时,溶液的pH=11.若反应后溶液的体积等于反应的两溶液的体积之和,则NaHSO4溶液与Ba(OH)2溶液的体积比为( )
| A、1:9 | B、1:1 |
| C、1:2 | D、1:4 |
摩尔是与阿伏加德罗常数直接相关的一个单位.若规定阿伏加德罗常数为0.024kg12C原子中所含碳原子的数目,则下列说法正确的是( )
| A、标准状况下气体的摩尔体积为22.4L |
| B、NH3的摩尔质量为17g/mol |
| C、18gH2O中约含有0.5mol水分子 |
| D、1L0.1mol/L的H2SO4溶液中含有0.1molSO42-离子 |
 对于N2O4(g)?2NO2(g)在温度一定时,平衡体系中NO2的体积分数V(NO2)%随压强的变化情况如图所示.
对于N2O4(g)?2NO2(g)在温度一定时,平衡体系中NO2的体积分数V(NO2)%随压强的变化情况如图所示.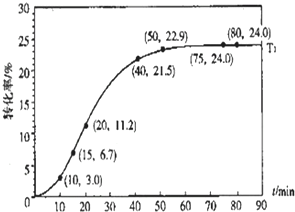 某种甲酸酯水解反应方程式为:
某种甲酸酯水解反应方程式为: 如图是硫酸试剂瓶标签上的内容
如图是硫酸试剂瓶标签上的内容 工业生产中用CO可以合成甲醇CO(g)+2H2(g)?CH3OH(g),△H=-90.1kJ?mol-1在一定压强下,容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图所示.
工业生产中用CO可以合成甲醇CO(g)+2H2(g)?CH3OH(g),△H=-90.1kJ?mol-1在一定压强下,容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图所示.