题目内容
2.Fe、Al分别与盐酸反应(结果可用分数表示):(1)若盐酸足量,等物质的量的Fe、Al产生H2的质量之比为2:3.
(2)若盐酸足量,等质量的Fe、Al产生H2的质量之比为9:28.
(3)若盐酸足量,等质量的Fe、Al产生H2在同温同压下的体积比为9:28.
分析 (1)若盐酸足量,Fe、Al均完全反应,失去电子数之比等于生成氢气的质量比;
(2)若盐酸足量,Fe、Al均完全反应,结合n=$\frac{m}{M}$及失去电子数之比等于生成氢气的质量比计算;
(3)若盐酸足量,Fe、Al均完全反应,结合n=$\frac{m}{M}$及失去电子数之比生成氢气的体积比计算.
解答 解:(1)若盐酸足量,Fe、Al均完全反应,设物质的量均为nmol,则等物质的量的Fe、Al产生H2的质量之比为n×(2-0):n×(3-0)=2:3,故答案为:2:3;
(2)若盐酸足量,Fe、Al均完全反应,设质量均为mg,则等质量的Fe、Al产生H2的质量之比为$\frac{m}{56}$×(2-0):$\frac{m}{27}$×(3-0)=9:28,故答案为:9:28;
(3)若盐酸足量,Fe、Al均完全反应,设质量均为mg,则等质量的Fe、Al产生H2在同温同压下的体积比为$\frac{m}{56}$×(2-0):$\frac{m}{27}$×(3-0)=9:28,故答案为:9:28.
点评 本题考查氧化还原反应的计算,为高频考点,把握酸足量时金属完全反应、电子守恒为解答的关键,侧重分析与计算能力的考查,注意氢气的物质的量比等于质量比也等于体积比,题目难度不大.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
19.下列物质中和苯互为同系物的是( )
| A. | 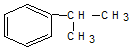 | B. | 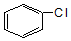 | C. | 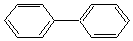 | D. | 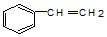 |
13.下列物质属于离子化合物的是( )
| A. | N2 | B. | NH3 | C. | HNO3 | D. | NH4Cl |
17.T℃时在2L恒容密闭容器中使X(g)与Y(g)发生反应生成Z(g).反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示.下列说法错误的是( )
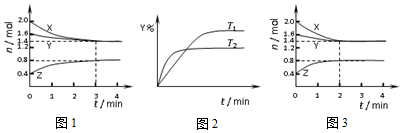

| A. | 容器中发生的反应可表示为:3X(g)+Y(g)?2Z(g) | |
| B. | 保持其他条件不变,升高温度,平衡向X体积分数增大的方向移动 | |
| C. | 反应进行的前3 min内,用X表示的反应速率 v(X)=0.2mol•(L•min)-1 | |
| D. | 若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂 |
7.某同学在实验报告中记录下列数据或操作,其中正确的是( )
| A. | 用100mL量筒量取8.6mL浓硫酸 | |
| B. | 用托盘天平称量8.75g食盐 | |
| C. | 用500mL的容量瓶来配制需要的450mL溶液 | |
| D. | 用胶头滴管取5mL的某溶液 |
11.一气球若放在空气中静止不动,那么在相同条件下该气体放在下列气体中会下沉的是( )
| A. | CH4 | B. | SO2 | C. | CO2 | D. | O2 |
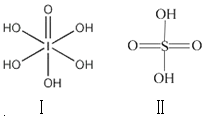 已知硫酸(H2SO4)和高碘酸(H5IO6)的结构分别如图I、II所示:请从结构角度比较二者酸性强弱:H2SO4>H5IO6(填“>”、“<”或“=”).
已知硫酸(H2SO4)和高碘酸(H5IO6)的结构分别如图I、II所示:请从结构角度比较二者酸性强弱:H2SO4>H5IO6(填“>”、“<”或“=”).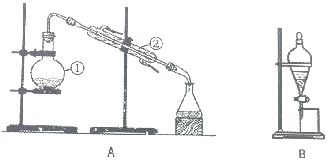 如图装置是实验室中物质分离的常用装置,请回答下列问题.
如图装置是实验室中物质分离的常用装置,请回答下列问题.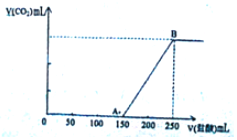 向100mL某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2,充分反应后,向所得溶液中逐滴滴入1mol/L的盐酸溶液,所得气体的体积(标准状态)与所加盐酸的体积关系如图所示
向100mL某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2,充分反应后,向所得溶液中逐滴滴入1mol/L的盐酸溶液,所得气体的体积(标准状态)与所加盐酸的体积关系如图所示