题目内容
13.将14g铜银合金与足量的HNO3反应,将产生的气体与1.12L O2(标准状况下)混合后,通入水中,恰好被全部吸收,则合金中Ag的质量为( )| A. | 3.2 g | B. | 4.8 g | C. | 6.4 g | D. | 10.8 g |
分析 铜、银合金与足量的某浓度的硝酸完全反应,反应生成氮的氧化物与1.12L的O2(标准状况)混合,通入水中,恰好完全吸收,纵观整个过程,金属提供电子物质的量等于氧气获得电子物质的量,令Cu、Ag的物质的量分别为xmol、ymol,根据二者质量及电子转移守恒列方程解答;
解答 解:14g铜、银合金与足量的某浓度的硝酸完全反应,反应生成氮的氧化物与1.12L的O2(标准状况)混合,通入水中,恰好完全吸收,纵观整个过程,金属提供电子物质的量等于氧气获得电子物质的量,令Cu、Ag的物质的量分别为xmol、ymol,根据二者质量及电子转移守恒,可得:
$\left\{\begin{array}{l}{64x+108y=14}\\{2x+y=\frac{1.12}{22.4}}\end{array}\right.$
解得x=0.05,y=0.1,
故m(Cu)=0.05mol×64g/mol=3.2g,m(Ag)=0.1mol×108g/mol=10.8g,
故选D.
点评 本题考查混合物计算、氧化还原反应的有关计算,难度中等,判断金属提供的电子等于氧气获得的电子是关键,注意氧化还原反应中守恒思想的运用.

练习册系列答案
相关题目
18.下列物质一定属于同系物的是( )
①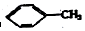 ②
②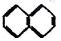 ③
③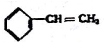 ④C2H4 ⑤CH2=CH-CH=CH2 ⑥C2H6 ⑦
④C2H4 ⑤CH2=CH-CH=CH2 ⑥C2H6 ⑦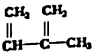 ⑧
⑧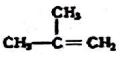
①
 ②
② ③
③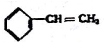 ④C2H4 ⑤CH2=CH-CH=CH2 ⑥C2H6 ⑦
④C2H4 ⑤CH2=CH-CH=CH2 ⑥C2H6 ⑦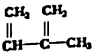 ⑧
⑧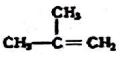
| A. | ④和⑧ | B. | ①、②和③ | C. | ⑤、⑦和⑧ | D. | ⑥和⑧ |
4.写出下列反应的热化学方程式:
(1)3mol NO2(g)与1mol H2O(l)反应生成HNO3(aq)和NO(g),放热138kJ.3NO2(g)+H2O(l)=2HNO3(aq)+NO(g)△H=-138kJ/mol;
(2)用CO还原1mol Fe2O3,放热24.8kJ.3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)△H=-24.8kJ/mol;
(3)1mol HgO(s)分解为液态汞和氧气,吸热90.7kJ.HgO(s)=Hg(l)+$\frac{1}{2}$O2(g)△H=+90.7kJ/mol;
(4)卫星发射时可用肼(N2H4)作燃料,1mol N2H4(l)在O2(g)中燃烧,生成N2(g)和H2O(l),放出622kJ热量:N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-622kJ/mol;
(5)6.4g液态甲醇(CH3OH)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式2CH3OH(1)+3O2(g)═2CO2(g)+4H2O(l)△H=-1135kJ/mol;
(6)已知反应N2+3H2?2NH3△H=a kJ•mol-1.试根据下表中所列键能数据估算a的数值为-93;
(7)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算.
已知:C(s,石墨)+O2(g)=CO2(g)△H1=-393.5kJ•mol-1
2H2(g)+O2(g)=2H2O(l)△H2=-571.6kJ•mol-1
2C2H2(g )+5O2(g)=4CO2(g)+2H2O(l)△H3=-2599kJ•mol-1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应的焓变△H=+226.7kJ•mol-1.
(1)3mol NO2(g)与1mol H2O(l)反应生成HNO3(aq)和NO(g),放热138kJ.3NO2(g)+H2O(l)=2HNO3(aq)+NO(g)△H=-138kJ/mol;
(2)用CO还原1mol Fe2O3,放热24.8kJ.3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)△H=-24.8kJ/mol;
(3)1mol HgO(s)分解为液态汞和氧气,吸热90.7kJ.HgO(s)=Hg(l)+$\frac{1}{2}$O2(g)△H=+90.7kJ/mol;
(4)卫星发射时可用肼(N2H4)作燃料,1mol N2H4(l)在O2(g)中燃烧,生成N2(g)和H2O(l),放出622kJ热量:N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-622kJ/mol;
(5)6.4g液态甲醇(CH3OH)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式2CH3OH(1)+3O2(g)═2CO2(g)+4H2O(l)△H=-1135kJ/mol;
(6)已知反应N2+3H2?2NH3△H=a kJ•mol-1.试根据下表中所列键能数据估算a的数值为-93;
| 化学键 | H-H | N-H | N≡N |
| 键能kJ/mol | 436 | 391 | 945 |
已知:C(s,石墨)+O2(g)=CO2(g)△H1=-393.5kJ•mol-1
2H2(g)+O2(g)=2H2O(l)△H2=-571.6kJ•mol-1
2C2H2(g )+5O2(g)=4CO2(g)+2H2O(l)△H3=-2599kJ•mol-1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应的焓变△H=+226.7kJ•mol-1.
1.某工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1mol•L-1.
甲同学欲探究废水的组成,进行了如下实验:
①用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察).
②取少量溶液,加入KSCN溶液无明显变化.
③另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变.
④向③中所得的溶液中加入BaCl2溶液,有白色沉淀生成.
请推断:
(1)由①、②、③判断,溶液中一定不含有的阳离子是K+、Fe3+,一定不含的阴离子是CO32-、SiO32-(写离子符号).
(2)③中加入少量盐酸生成无色气体的离子方程式是3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,④中生成白色沉淀的离子方程式是SO42-+Ba2+=BaSO4↓.
(3)将③中所得红棕色气体通入水中,气体变无色,所发生的化学反应方程式为3NO2+H2O=2HNO3+NO.
(4)甲同学最终确定原溶液中所含阳离子是Fe2+、Mg2+,阴离子是Cl-、NO3-、SO42-.(写离子符号)
| 阳离子 | K+ Mg2+ Fe3+ Al3+ Fe2+ |
| 阴离子 | Cl-CO32- NO3- SO42- SiO32- |
①用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察).
②取少量溶液,加入KSCN溶液无明显变化.
③另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变.
④向③中所得的溶液中加入BaCl2溶液,有白色沉淀生成.
请推断:
(1)由①、②、③判断,溶液中一定不含有的阳离子是K+、Fe3+,一定不含的阴离子是CO32-、SiO32-(写离子符号).
(2)③中加入少量盐酸生成无色气体的离子方程式是3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,④中生成白色沉淀的离子方程式是SO42-+Ba2+=BaSO4↓.
(3)将③中所得红棕色气体通入水中,气体变无色,所发生的化学反应方程式为3NO2+H2O=2HNO3+NO.
(4)甲同学最终确定原溶液中所含阳离子是Fe2+、Mg2+,阴离子是Cl-、NO3-、SO42-.(写离子符号)
8.某无色水溶液可能含有以下离子中的若干种:NH4+、Cl-、Fe2+、Ba2+、K+、CO32-、SO42-,现取三份100mL 的该溶液进行如下实验:①第一份加入AgNO3溶液有沉淀产生;②第二份加足量NaOH溶液加热后,收集到气体0.04mol; ③第三份加足量BaCl2溶液后,得干燥沉淀6.27g,用足量盐酸洗涤、干燥后,剩余沉淀质量为2.33g.根据上述实验结果推测以下说法不正确的是( )
| A. | K+一定存在 | B. | 溶液中CO32-浓度为0.1 mol/L | ||
| C. | Cl-可能存在 | D. | Ba2+一定不存在 |
18.在一个绝热的容积固定的密闭容器中发生可逆反应:mA(g)+nB(g)?pC(g)+qD(g),当 m、n、p、q 为任意整数时,反应达到平衡的标志是:①体系的密度不再改变,②体系的温度不再改变,③A 的转化率不再改变,④各组分的百分含量不再改变,⑤反应 速率,v(A):v(B):v(C):v(D)=m:n:p:q.下列组合完全正确的是( )
| A. | ②③④ | B. | ①③⑤ | C. | ②④⑤ | D. | ①②③④⑤ |
2.化学科学需要借助化学专用语言描述,下列有关化学用语书写正确的是( )
| A. | CO2的电子式 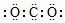 | B. | Cl-的结构示意图 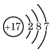 | ||
| C. | HCl的电子式 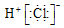 | D. | 质量数为37的氯原子${\;}_{17}^{37}$Cl |