题目内容
9.请根据所学知识回答下列问题:(1)同温同压下,H2(g)+Cl2(g)═2HCl(g),在光照和点燃条件下的△H(化学计量数相同)分别为△H1、△H2,△H1 =△H2(填“>”、“<”或“=”,下同).
(2)相同条件下,2mol氢原子所具有的能量>1mol氢分子所具有的能量.
(3)已知常温时红磷比白磷稳定,比较下列反应中△H的大小:△H1<△H2.
①P4(白磷,s)+5O2(g)═2P2O5(s)△H1,
②4P(红磷,s)+5O2(g)═2P2O5(s)△H2.
(4)已知:稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1,则浓硫酸与稀氢氧化钠溶液反应生成1mol水,放出的热量>57.3kJ.
(5)已知:0.5mol CH4(g)与0.5mol水蒸气在t℃、p kPa时,完全反应生成CO和H2的混合气体,吸收了a kJ热量,该反应的热化学方程式是CH4(g)+H2O(g)=CO(g)+3H2(g),△H=+2akJ/mol.
分析 (1)反应热与反应物的总能量和生成物的总能量,与反应条件无关;
(2)化学键断裂为吸热过程,新键生成放热的过程;
(3)常温时红磷比白磷稳定,说明白磷能量高,反应放出的热量较多;
(4)浓硫酸溶于水放热;
(5)根据热化学方程式的含义以及书写方法来回答.
解答 解:(1)反应热与反应物的总能量和生成物的总能量,与反应条件无关,则光照和点燃条件的△H相同;
故答案为:=;
(2)氢气分子生成氢原子要破坏化学键,需要吸热,则2mol氢原子所具有的能量大于1mol氢分子所具有的能量;
故答案为:>;
(3)常温时红磷比白磷稳定,说明白磷能量高,反应放出的热量较多,因△H<0,则放出的能量越多反应热越小;
故答案为:<;
(4)浓硫酸溶于水放热,放出的热量大于57.3kJ;
故答案为:>;
(5)甲烷和水蒸气之间的反应方程式为:CH4(g)+H2O(g)=CO(g)+3H2(g),0.5mol甲烷与0.5mol水蒸气在t℃、p kPa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量,所以1mol甲烷与1mol水蒸气在t℃、p kPa时,完全反应生成一氧化碳和氢气(合成气),吸收了2a kJ热量,热化学方程式为:CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+2akJ/mol;
故答案为:$\frac{1}{2}$CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+2akJ/mol.
点评 本题综合考查反应热的大小比较以及影响化学平衡的因素,题目难度不大,注意把握比较反应热的角度.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.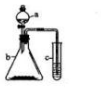 利用右下图所示的装置进行实验,将仪器a中的溶液滴入b中,根据c中所盛溶液,预测c中现象正确的是( )
利用右下图所示的装置进行实验,将仪器a中的溶液滴入b中,根据c中所盛溶液,预测c中现象正确的是( )
 利用右下图所示的装置进行实验,将仪器a中的溶液滴入b中,根据c中所盛溶液,预测c中现象正确的是( )
利用右下图所示的装置进行实验,将仪器a中的溶液滴入b中,根据c中所盛溶液,预测c中现象正确的是( )| 选项 | a | b | c | c试管中的现象 |
| A | 浓盐酸 | KMnO4 | FeCl2溶液 | 溶液变棕黄色 |
| B | 稀硫酸 | Na2S2O3 | 溴水 | 产生浅黄色沉淀 |
| C | 饱和NaCl | CaC2 | 硫酸铜溶液 | 产生蓝色沉淀 |
| D | 浓硝酸 | 铁片 | KI-淀粉溶液 | 溶液变蓝色 |
| A. | A | B. | B | C. | C | D. | D |
18.A、B、C、D、E六种物质的转化关系如图所示(未标出反应条件),A、D、F都是由短周期非金属元素形成的单质,B、C、E都是二元化合物.A、F所含元素同周期,下列说法不正确的是( )

| A. | A、D所含元素的原子序数大小:A一定比D小 | |
| B. | A、F所含元素的原子半径大小:A一定比F大 | |
| C. | B、E含有化学键类型相同 | |
| D. | 若常温下D为固体,则B可以与NaOH溶液反应 |
14. 如图装置,a为铁电极,b为石墨电极,烧杯中的物质为水或某种溶液,两电极可直接相连或接直流电源,则石墨电极上可能发生的反应有( )
如图装置,a为铁电极,b为石墨电极,烧杯中的物质为水或某种溶液,两电极可直接相连或接直流电源,则石墨电极上可能发生的反应有( )
①2H++2e-═H2 ②O2+2H2O+4e-═4OH-③4OH-═O2+2H2O+4e-.
 如图装置,a为铁电极,b为石墨电极,烧杯中的物质为水或某种溶液,两电极可直接相连或接直流电源,则石墨电极上可能发生的反应有( )
如图装置,a为铁电极,b为石墨电极,烧杯中的物质为水或某种溶液,两电极可直接相连或接直流电源,则石墨电极上可能发生的反应有( )①2H++2e-═H2 ②O2+2H2O+4e-═4OH-③4OH-═O2+2H2O+4e-.
| A. | ① | B. | ② | C. | ①② | D. | ①②③ |
1.下列各项中,不能运用化学平衡移动原理解释的是( )
| A. | 实验室中用饱和食盐水除去氯气中的氯化氢气体 | |
| B. | 实验室中久置的浓氨水碱性减弱 | |
| C. | 向硝酸亚铁溶液中滴加盐酸,溶液变为黄色 | |
| D. | 在较高温度下测定二氧化氮气体相对分子质量 |
18.在一个定容的密闭容器中进行如下反应:2SO2(g)+O2(g)?2SO3(g).已知反应过程中的某一时间SO2、O2和SO3的浓度分别为0.1mol•L-1、0.05mol•L-1和0.3mol•L-1.当反应达平衡时不可能存在的数据正确的是( )
| A. | c(SO2)=0.25 mol•L-1 | B. | c(O2)=0.12 mol•L-1 | ||
| C. | c(SO2)+c(SO3)=0.15 mol•L-1 | D. | c(SO3)+c(O2)=0.3 mol•L-1 |
19.合成导电高分子材料PPV的反应: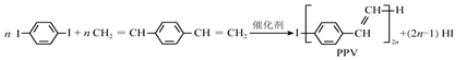
下列说法正确的是( )
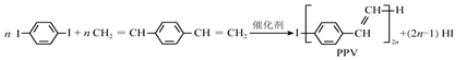
下列说法正确的是( )
| A. | 合成PPV的反应为加聚反应 | |
| B. | PPV与聚苯乙烯具有相同的重复结构单元 | |
| C. | H2C═CH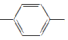 CH═CH2和苯乙烯互为同系物 CH═CH2和苯乙烯互为同系物 | |
| D. | 通过质谱法测定PPV的平均相对分子质量,可得其聚合度 |
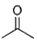 根据键线式回答下列问题:
根据键线式回答下列问题: 分子式:C5H9O2,结构简式:CH2=C(CH3)COOCH3
分子式:C5H9O2,结构简式:CH2=C(CH3)COOCH3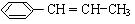 )在催化剂作用下生成聚苯丙烯的反应方程式:
)在催化剂作用下生成聚苯丙烯的反应方程式:
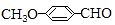 有多种的同分异构体,其中属于芳香族羧酸的同分异构体共有4种,它们的结构简式是:
有多种的同分异构体,其中属于芳香族羧酸的同分异构体共有4种,它们的结构简式是: ;
; ;
; ,
, (任意一种);、(任写其中一种)
(任意一种);、(任写其中一种)