题目内容
9.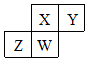 短周期元素X、Y、Z、W在元素周期表中的相对位置如表所示,W原子的质子数是其最外层电子数的三倍.下列说法不正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如表所示,W原子的质子数是其最外层电子数的三倍.下列说法不正确的是( )| A. | 元素Y有同素异形体 | |
| B. | 最高价氧化物对应水化物的酸性:X>Z | |
| C. | 简单气态氢化物的热稳定性:Y>Z | |
| D. | 原于半径:W>Z>Y>X |
分析 由短周期元素X、Y、Z、W在元素周期表中的相对位置,可知W位于第三周期,W原子的质子数是其最外层电子数的三倍,设最外层电子数为x,则10+x=3x,解得x=5,可知W为P,结合元素的位置可知,Z为Si,X为N,Y为O,以此来解答.
解答 解:由上述分析可知,X为N,Y为O,Z为Si,W为P,
A.Y存在氧气、臭氧,互为同素异形体,故A正确;
B.非金属性N>Si,最高价氧化物对应水化物的酸性:X>Z,故B正确;
C.非金属性O>Si,简单气态氢化物的热稳定性:Y>Z,故C正确;
D.电子层越多,原子半径越大,同周期从左向右原子半径减小,则原于半径:Z>W>X>Y,故D错误;
故选D.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子结构、元素的位置推断元素为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
相关题目
20.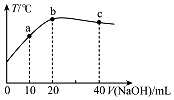 在一隔热系统中,向20.00mL 0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol.L-1的NaOH溶液,测得混合溶液的温度变化如图.下列相关说法正确的是( )
在一隔热系统中,向20.00mL 0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol.L-1的NaOH溶液,测得混合溶液的温度变化如图.下列相关说法正确的是( )
 在一隔热系统中,向20.00mL 0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol.L-1的NaOH溶液,测得混合溶液的温度变化如图.下列相关说法正确的是( )
在一隔热系统中,向20.00mL 0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol.L-1的NaOH溶液,测得混合溶液的温度变化如图.下列相关说法正确的是( )| A. | 若a点溶液呈酸性,此时:c(CH3COO-)-c(CH3COOH)=2c(H+)-2c(OH-) | |
| B. | B.从a到b:$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$逐渐增大 | |
| C. | 水的电离程度:b点<c点 | |
| D. | 溶液的pH值:a点<c点<b点 |
4.已知HF 酸性强于CH3COOH,常温下有下列三种溶液.有关叙述不正确的是( )
| 编号 | ① | ② | ③ |
| PH | 11 | 3 | 3 |
| 溶液 | NaOH溶液 | CH3COOH溶液 | HF溶液 |
| A. | CH3COOH稀溶液中加入少量CH3COONa,能使比值c(CH3COO-)/c(Na+)增大 | |
| B. | ①、②等体积很合后:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| C. | 向②加入NaF固体,CH3COOH电离平衡正向移动 | |
| D. | 中和相同体积的②、③,需消耗①的体积②<③ |
14.下列现象属于物理变化的是( )
| A. | 潮解 | B. | 电解 | C. | 水解 | D. | 裂解 |
1.升高温度,下列数据不一定增大的是( )
| A. | 化学反应速率v | B. | 弱电解质的电离度α | ||
| C. | 化学平衡常数K | D. | 水的离子积常数Kw |
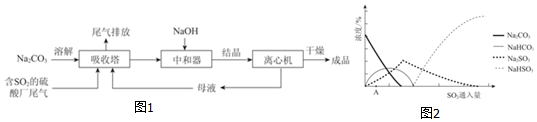
18.二氧化氯(ClO2)是极易溶于水且不与水发生化学反应的黄绿色气体,沸点为 11℃,可用于处理含硫废水.某小组在实验室中探究 ClO2 与 Na2S 的反应.回答下列问题:
(1)ClO2 的制备
已知:SO2+2NaClO3+H2SO4═2ClO2↑+2NaHSO4
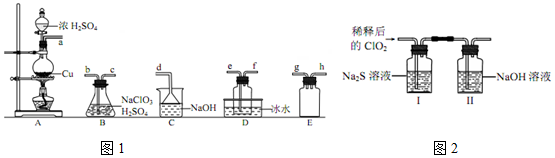
①装置 A 中反应的化学方程式为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+H2O.
②欲收集干燥的 ClO2,选择图1中的装置,其连接顺序为 a→g→h→b→c→e→f→d(按气流方向,用小写字母表示)
③装置 D 的作用是冷凝并收集ClO2.
(2)ClO2 与 Na2S 的反应
将上述收集到的 ClO2 用 N2 稀释以增强其稳定性,并将适量的稀释后的 ClO2 通入如图2所示装置中充分反应,得到无色澄清溶液.一段时间后,通过下列实验探究 I 中反应的产物.
④ClO2 与 Na2S 反应的离子方程式为8ClO2+5S2-+4H2O=8Cl-+5SO42-+8H+.用于处理含硫废水时,ClO2 相对于Cl2 的优点是ClO2除硫效果彻底,氧化产物硫酸根更稳定、ClO2在水中的溶解度大、剩余的ClO2不会产生二次污染、均被还原为氯离子时,ClO2得到的电子数是氯气的2.5倍(任写一条).
(1)ClO2 的制备
已知:SO2+2NaClO3+H2SO4═2ClO2↑+2NaHSO4

①装置 A 中反应的化学方程式为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+H2O.
②欲收集干燥的 ClO2,选择图1中的装置,其连接顺序为 a→g→h→b→c→e→f→d(按气流方向,用小写字母表示)
③装置 D 的作用是冷凝并收集ClO2.
(2)ClO2 与 Na2S 的反应
将上述收集到的 ClO2 用 N2 稀释以增强其稳定性,并将适量的稀释后的 ClO2 通入如图2所示装置中充分反应,得到无色澄清溶液.一段时间后,通过下列实验探究 I 中反应的产物.
| 操作步骤 | 实验现象 | 结论 |
| 取少量I中溶液于试管甲中,滴加品红溶液和盐酸 | 品红始终不褪色 | ①无SO2(或HSO3-或SO32-)生成 |
| 另取少量I中溶液于试管乙中,加入Ba(OH)2溶液,振荡 | ②白色沉淀 | 有SO42-生成 |
| ③继续在试管乙中滴加Ba(OH)2溶液至过量,静置,取上层清液于试管丙内 加入足量稀硝酸酸化的硝酸银溶液 | 有白色沉淀生成 | 有Cl-生成 |
19.化学与生产、生活、科技、环境等密切相关,下列说法错误的是( )
| A. | 利用CO2合成聚碳酸酯可降解塑料,实现“碳”的循环利用 | |
| B. | 氯水中加入稀硫酸,可增强氯水的漂白性 | |
| C. | 用蘸有浓氨水的玻璃棒检验输送氯气的管道是否漏气 | |
| D. | 加工后具有吸水性的植物纤维可用作食品干燥剂 |