题目内容
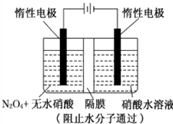 如图所示装置可通过发生“3N2O4+8HNO3=6N2O5+2NO+4H2O”制备N2O5,有关说法中错误的是( )
如图所示装置可通过发生“3N2O4+8HNO3=6N2O5+2NO+4H2O”制备N2O5,有关说法中错误的是( )| A、阴极的电极反应为:NO3-+4H++3e-=NO↑+2H2O |
| B、阳极的电极反应为:N2O4+2 HNO3-2e-=2N2O5+2H+ |
| C、当电路中通过6 mol e-时整个电解池中参与反应的HNO3为8mol |
| D、当电路中通过6 mol e-时,有8molH+从阳极向阴极迁移 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:在反应3N2O4+8HNO3=6N2O5+2NO+4H2O中,阳极上N2O4发生氧化反应,生成N2O5,每摩N2O4反应转移电子2mol;HNO3在阴极发生还原反应,生成NO,每摩HNO3反应转移电子3mol,电解质溶液为酸性环境,可以形成电极反应式,据此解答.
解答:
解:在反应3N2O4+8HNO3=6N2O5+2NO+4H2O中,阳极上N2O4发生氧化反应,生成N2O5,每摩N2O4反应转移电子2mol;HNO3在阴极发生还原反应,生成NO,每摩HNO3被还原时转移电子3mol,电解质溶液为酸性环境,可以形成电极反应式,
A、阴极发生还原反应,电极反应式为:NO3-+4H++3e-=NO↑+2H2O,故A正确;
B、阳极发生还原反应,电极反应式为:N2O4+2 HNO3-2e-=2N2O5+2H+,故B正确;
C、从反应方程式可见,每8mol硝酸反应,只有2mol被还原,转移6mol电子,故C正确;
D、依据电荷守恒,当电路中通过6 mol e-时,应有6molH+从阳极向阴极迁移,故D错误.
故选D.
A、阴极发生还原反应,电极反应式为:NO3-+4H++3e-=NO↑+2H2O,故A正确;
B、阳极发生还原反应,电极反应式为:N2O4+2 HNO3-2e-=2N2O5+2H+,故B正确;
C、从反应方程式可见,每8mol硝酸反应,只有2mol被还原,转移6mol电子,故C正确;
D、依据电荷守恒,当电路中通过6 mol e-时,应有6molH+从阳极向阴极迁移,故D错误.
故选D.
点评:本题主要考查电解池的工作原理,注意阳极发生氧化反应,阴极发生还原反应,并注意电子守恒和电荷守恒.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
下列说法中正确的是( )
| A、摩尔既是物质的数量单位又是物质的质量单位 |
| B、物质的量既表示物质的数量又表示物质的质量 |
| C、阿伏加德罗常数是12 kg 12C中含有的碳原子数目 |
| D、1 mol H2O中含有2 mol H原子和1mol O原子 |
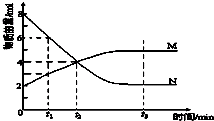 一定温度下在2L的密闭容器内进行反应,M、N的物质的量随反应时间变化的曲线如图,下列表述正确的是( )
一定温度下在2L的密闭容器内进行反应,M、N的物质的量随反应时间变化的曲线如图,下列表述正确的是( )| A、反应的化学方程式:2M?N |
| B、t2时,正、逆反应速率相等,达到平衡 |
| C、平衡时,N的转化率为75% |
| D、若t1=2min,用N的浓度表示的化学反应速率为0.5 mol?(L?s)-1 |
下列叙述中不 正确的是( )
| A、石英沙、水晶的主要成分都是SiO2 |
| B、SiO2是制光导纤维的主要原料 |
| C、石灰石是制普通玻璃、水泥的原料之一 |
| D、SiO2与水反应直接制得硅酸 |
下列各组性质比较中,正确的是( )
①酸性:HClO4>HBrO4>HIO4
②离子还原性:S2->Cl->Br->I-
③沸点:HF>HCl>HBr>HI
④金属性:K>Na>Mg>Al
⑤气态氢化物稳定性:HF>HCl>H2S
⑥半径:O2->Na+>Na>Cl.
①酸性:HClO4>HBrO4>HIO4
②离子还原性:S2->Cl->Br->I-
③沸点:HF>HCl>HBr>HI
④金属性:K>Na>Mg>Al
⑤气态氢化物稳定性:HF>HCl>H2S
⑥半径:O2->Na+>Na>Cl.
| A、①②③ | B、②③④ |
| C、①④⑤ | D、①②③④⑤⑥ |
硝酸铵(NH4NO3)在不同条件下分解可得到不同的产物,下列各组物质中肯定不可能是硝酸铵分解产物的是( )
| A、HNO3、NO、H2O |
| B、N2、HNO3、H2O |
| C、N2、O2、H2O |
| D、N2O、H2O |
下列有关化学能与热能的说法错误的是( )
| A、燃烧反应都属于放热反应 |
| B、化学反应必然伴随着能量的变化 |
| C、吸热反应是指需要加热才能进行的反应 |
| D、化学键的断裂和形成是化学反应中能量变化的主要原因 |
下列说法不正确的是( )
| A、二氧化硅是制造光导纤维的材料,单质硅是良好的半导体材料 |
| B、SiO2和CO2都是酸性氧化物,但SiO2不能和水反应生成硅酸 |
| C、保存NaOH溶液时不能用玻璃塞 |
| D、二氧化硅性质稳定,不与任何酸反应 |
下列说法正确的是( )
| A、HF、HCl、HBr、HI的热稳定性依次减弱,沸点却依次升高 |
| B、熔融状态下能导电的化合物一定含离子键 |
| C、H2O2分子中所有的原子均为8电子稳定结构 |
| D、NaHSO4晶体中阴、阳离子的个数是1:2且熔化时破坏的是离子键和共价键 |