题目内容
 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )| A、原子半径:rW>rZ>rY>rX |
| B、Y元素的氧化物不能与烧碱溶液反应 |
| C、气态氢化物的热稳定性:Z>W |
| D、X与氢元素组成的化合物XH5与水反应可产生两种气体 |
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:短周期元素X、Y、Z、W,W原子的最外层电子数是最内层电子数的3倍,若为2个电子层,则W的最外层电子数为6,所以W为O,由位置可知,不符合题意;若为3个电子层,则W的最外层电子数为6,所以W为S,由位置可知,X为N,Y为Al,Z为Si,结合元素及其单质、化合物的性质来解答.
解答:
解:短周期元素X、Y、Z、W,W原子的最外层电子数是最内层电子数的3倍,若为2个电子层,则W的最外层电子数为6,所以W为O,由位置可知,不符合题意;若为3个电子层,则W的最外层电子数为6,所以W为S,由位置可知,X为N,Y为Al,Z为Si,
A.电子层越多,半径越大,具有相同电子层的原子序数越大其原子半径越小,则原子半径为rY>rZ>rW>rX,故A错误;
B.Y为Al,氧化铝为两性氧化物,能与烧碱溶液反应,故B错误;
C.非金属性W>Z,则最简单气态氢化物的热稳定性为W>Z,故C错误;
D.X为N,X与氢元素组成的化合物XH5与水反应可产生氨气、氢气两种气体,故D正确;
故选D.
A.电子层越多,半径越大,具有相同电子层的原子序数越大其原子半径越小,则原子半径为rY>rZ>rW>rX,故A错误;
B.Y为Al,氧化铝为两性氧化物,能与烧碱溶液反应,故B错误;
C.非金属性W>Z,则最简单气态氢化物的热稳定性为W>Z,故C错误;
D.X为N,X与氢元素组成的化合物XH5与水反应可产生氨气、氢气两种气体,故D正确;
故选D.
点评:本题考查结构性质位置关系应用,为高频考点,侧重于学生的分析能力的考查,W为推断的突破口,注意D选项知识中学基本不接触,为本题难点,注意根据水解反应进行理解,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
只用一种试剂就能将甘油、苯酚溶液、四氯化碳、己烯、苯五种无色液体分开的是( )
| A、FeCl3溶液 |
| B、NaOH溶液 |
| C、溴水 |
| D、镁 |
纳米是长度单位,1纳米等于1×10-9米,物质的颗粒达到纳米级时,具有特殊的性质.例如将单质铜制成“纳米铜”时,具有非常强的化学活性,在空气中可以燃烧.下列对“纳米铜”的有关叙述正确的是( )
| A、常温下“纳米铜”比铜片的还原性强,反应时反应速率快 |
| B、“纳米铜”颗粒更细小,化学反应时接触面大,所以反应速率快 |
| C、“纳米铜”与铜是同素异形体 |
| D、常温下“纳米铜”比铜片更易得电子,反应时反应速率快 |
下列表示对应化学反应的离子方程式正确的是( )
A、MnO2 与浓盐酸反应制Cl2:MnO2+4HCl
| ||||
| B、铜与稀硝酸反应:Cu+4H++2NO3-═2H2O+Cu2++2NO2↑ | ||||
| C、足量氨水吸收少量二氧化硫气体:NH3?H2O+SO2=NH4++HSO3- | ||||
| D、Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
下列物质中,在一定条件下既能发生银镜反应,又能发生水解和氧化反应的是( )
| A、乙酸甲酯 | B、溴乙烯 |
| C、甲酸乙酯 | D、苯甲醛 |
下列物质均有漂白性,其中漂白原理与其他三种不同的是( )
| A、HClO |
| B、SO2 |
| C、O3 |
| D、Na2O2 |
 与
与  ⑥CH3-CH2-OH和CH3-O-CH3
⑥CH3-CH2-OH和CH3-O-CH3 相对分子质量为174的有机物M中只含有C、H、O三种元素,其分子结构如图所示.请回答下列问题:
相对分子质量为174的有机物M中只含有C、H、O三种元素,其分子结构如图所示.请回答下列问题: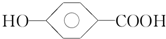 ,该反应的化学方程式是
,该反应的化学方程式是