题目内容
一定量的盐酸跟过量的铁粉反应时,为了减缓反应速度,且不影响生成氢气的总量,可向盐酸中加入适量的( )
①NaOH固体 ②少许H2O ③升温 ④CH3COONa固体 ⑤降温 ⑥KCl溶液.
①NaOH固体 ②少许H2O ③升温 ④CH3COONa固体 ⑤降温 ⑥KCl溶液.
| A、②④⑤⑥ | B、①② |
| C、②③⑤ | D、②⑤⑥ |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:Fe过量,生成氢气由盐酸决定,为了减缓反应速度,且不影响生成氢气的总量,减小氢离子浓度不改变其物质的量即可,以此来解答.
解答:
解:①NaOH固体,与盐酸反应,生成氢气的量减少,故不选;
②H2O,对盐酸稀释,氢离子浓度减小但物质的量不变,故选;
③升温,活化分子百分数增大,反应速率增大,故不选;
④CH3COONa固体,生成醋酸,氢离子浓度减小但物质的量不变,故选;
⑤降温,反应速率减小,且不影响生成氢气的总量,故选;
⑥KCl溶液,相当于对盐酸稀释,氢离子浓度减小但物质的量不变,故选;
故选A.
②H2O,对盐酸稀释,氢离子浓度减小但物质的量不变,故选;
③升温,活化分子百分数增大,反应速率增大,故不选;
④CH3COONa固体,生成醋酸,氢离子浓度减小但物质的量不变,故选;
⑤降温,反应速率减小,且不影响生成氢气的总量,故选;
⑥KCl溶液,相当于对盐酸稀释,氢离子浓度减小但物质的量不变,故选;
故选A.
点评:本题考查影响化学反应速率的因素,明确浓度对反应速率的影响即可解答,注意Fe过量,改变浓度是关键,题目难度不大.

练习册系列答案
相关题目
由二氧化硅制高纯硅的流程图如图,下列判断中错误的是( )
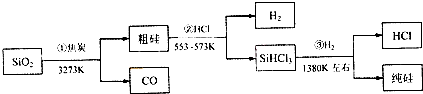

| A、①②③均属于氧化还原反应 |
| B、H2和HCl均可循环利用 |
| C、SiO2是一种坚硬难熔的固体 |
| D、光纤的主要成分是高纯度的单质硅 |
如图实验装置或操作与微粒的大小无直接关系的是( )
A、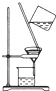 过滤 |
B、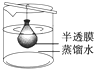 渗析 |
C、 萃取 |
D、 丁达尔效应 |
下列表达方式正确的是( )
| A、乙烯的结构简式CH2CH2 |
B、基态氧原子L层电子排布图: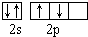 |
C、甲基的电子式 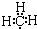 |
| D、HClO的结构式:H-Cl-O |
在一定密闭容器中,反应aA(g)═bB(g)达平衡后,保持温度及各物质的量不变,将容器体积增加1倍,当达到新平衡时,B的浓度是原来的60%,则下列说法不正确的是( )
| A、平衡向正反应方向移动了 |
| B、物质A的转化率减少了 |
| C、容器体积增加可以是向其中充入了惰性气体 |
| D、a<b |