题目内容
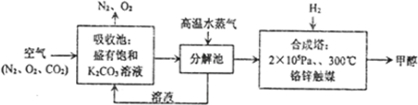
近几年来,我国中东部地区陷入严重的雾霾天气,面对全球近期的气候异常,环境问题再次成为焦点.非金属氧化物的合理控制和治理是优化我们生存环境的有效途径之一.请运用化学反应原理知识,回答下列问题:
目前,消除氮氧化物污染有多种方法.
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染.已知:
①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H═-574kJ.mol-1
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H═-1160.mol-1
③H2O(g)=H2O(Ⅰ)△H=-44.0kJ.mol-1写出CH4(g)与NO2(g)反应生成N2(g),CO2(g)和H2O(l)H2O的热化学方程式 .
(2)用活性炭还原法处理氮氧化物.有关反应为:C(s)+2NO(g)?N2(g)+CO2(g)某研究小组向恒容密闭容器中加入一定量的活性炭和NO,恒温(T℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
①T℃时该反应的平衡常数为 (结果保留两位有效数字).
②30min后改变某一条件,反应重新达到平衡,则改变的条件可能是 .
③若30min后升高温度重新达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则该反应△H 0(填“<”“>”“=”).
目前,消除氮氧化物污染有多种方法.
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染.已知:
①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H═-574kJ.mol-1
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H═-1160.mol-1
③H2O(g)=H2O(Ⅰ)△H=-44.0kJ.mol-1写出CH4(g)与NO2(g)反应生成N2(g),CO2(g)和H2O(l)H2O的热化学方程式
(2)用活性炭还原法处理氮氧化物.有关反应为:C(s)+2NO(g)?N2(g)+CO2(g)某研究小组向恒容密闭容器中加入一定量的活性炭和NO,恒温(T℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
| 浓度(mol/L) 时间(min) | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
②30min后改变某一条件,反应重新达到平衡,则改变的条件可能是
③若30min后升高温度重新达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则该反应△H
考点:化学平衡的计算,热化学方程式,化学平衡的影响因素
专题:
分析:(1)根据盖斯定律计算得到所需热化学方程式,标注物质聚集状态和对应反应焓变;
(2)①20min-30min反应达到平衡,图表中平衡浓度,依据平衡常数的概念计算得到;
②依据图表数据变化分析,30min末一氧化氮和二氧化碳浓度减小,氮气浓度增大,结合计算平衡常数和浓度变化分析判断;改变的条件可能是减小二氧化碳浓度;
③根据浓度比值的变化来确定移动方向.
(2)①20min-30min反应达到平衡,图表中平衡浓度,依据平衡常数的概念计算得到;
②依据图表数据变化分析,30min末一氧化氮和二氧化碳浓度减小,氮气浓度增大,结合计算平衡常数和浓度变化分析判断;改变的条件可能是减小二氧化碳浓度;
③根据浓度比值的变化来确定移动方向.
解答:
解:(1)①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJ?mol-l
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2 O(g)△H=-1160kJ?mol-l
③H2O(g)═H2O(l)△H=-44.0kJ?mol-l
依据盖斯定律计算[①+②+③×4]×
得到CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l)△H=-955 kJ?mol-1;
故答案为:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l)△H=-955 kJ?mol-1;
(2)①20-30min反应达到平衡状态,C(s)+2NO(g)?N2 (g)+CO2 (g),各物质的平衡浓度为:c(CO2)=c(N2)=0.3mol/L;c(NO)=0.4mol/L,反应的平衡常数为:K=
=
=0.56,故答案为:0.56;
②30min时改变某一条件,反应重新达到平衡时c(N2)=0.34mol/L;c(CO2)=0.17mol/L;c(NO)=0.32mol/L;则平衡常数K=
=
=0.56,平衡常数不变说明改变的条件一定不是温度;依据数据分析,氮气浓度增大,二氧化碳和一氧化氮浓度减小,反应前后气体体积不变,所以减小二氧化碳浓度,平衡正向进行的结果,故答案为:减小二氧化碳浓度;
③30min时,容器中NO、N2、CO2的浓度之比=0.040:0.030:0.030=4:3:3,30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则平衡向逆反应方向移动,所以逆反应是吸热反应,正反应是放热反应,则△H<0,故答案为:<.
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2 O(g)△H=-1160kJ?mol-l
③H2O(g)═H2O(l)△H=-44.0kJ?mol-l
依据盖斯定律计算[①+②+③×4]×
| 1 |
| 2 |
故答案为:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l)△H=-955 kJ?mol-1;
(2)①20-30min反应达到平衡状态,C(s)+2NO(g)?N2 (g)+CO2 (g),各物质的平衡浓度为:c(CO2)=c(N2)=0.3mol/L;c(NO)=0.4mol/L,反应的平衡常数为:K=
| c(CO 2)c(N 2) |
| c 2(NO) |
| 0.3×0.3 |
| 0.42 |
②30min时改变某一条件,反应重新达到平衡时c(N2)=0.34mol/L;c(CO2)=0.17mol/L;c(NO)=0.32mol/L;则平衡常数K=
| c(CO 2)c(N 2) |
| c 2(NO) |
| 0.34×0.17 |
| 0.32 2 |
③30min时,容器中NO、N2、CO2的浓度之比=0.040:0.030:0.030=4:3:3,30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则平衡向逆反应方向移动,所以逆反应是吸热反应,正反应是放热反应,则△H<0,故答案为:<.
点评:本题考查了化学平衡常数、化学平衡移动的影响因素等,侧重考查学生对数据的分析处理,题目难度中等.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
下列关于如图所示有机物的说法中,不正确的是( )
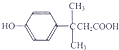

| A、该物质能发生缩聚反应 |
| B、该物质的核磁共振氢谱上共有7个峰 |
| C、该物质能与浓溴水发生反应 |
| D、1mol该物质完全反应最多消耗Na、NaOH、NaHCO3的物质的量之比为2:2:1 |
下列说法中,不正确的是( )
| A、反应热指的是反应过程中吸收或放出的热量 |
| B、原电池的负极发生氧化反应 |
| C、伴随能量变化的不一定是化学变化 |
| D、电解池的阳极发生氧化反应 |
Zn与稀HNO3反应的物质的量之比为5:12,氧化产物为硝酸锌,则HNO3被还原的产物为( )
| A、NO |
| B、NO2 |
| C、N2 |
| D、N2O3 |
下列结论正确的是( )
| A、向氯化铝溶液中滴加过量氨水,反应的离子方程式是:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| B、足量铜与含1mol溶质的浓硫酸反应,可生成0.5molSO2 |
| C、溶液与胶体:本质不同的原因是能否发生丁达尔效应 |
| D、15.6g过氧化钠与足量二氧化碳充分反应,转移电子数为1.204×1023 |
在核反应方程
He+
N→
O+X中,X代表的粒子是( )
4 2 |
14 7 |
17 8 |
A、
| ||
B、
| ||
C、
| ||
D、
|
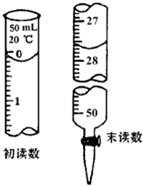 “学生甲”通过中和滴定的方法,去测定在空气中露置一段时间后的NaOH固体的纯度,设计如下方案:
“学生甲”通过中和滴定的方法,去测定在空气中露置一段时间后的NaOH固体的纯度,设计如下方案: