题目内容
17.某元素R的最高价氧化物的水化物分子式是H3RO4,则在气态氢化物中R元素的化合价是( )| A. | -1 | B. | -2 | C. | -3 | D. | -4 |
分析 根据最高价氧化物对应的水化物的化学式可知元素的最高正价,再利用最高正化合价-8=最低负价,则可知最低负价,由此分析解答.
解答 解:R元素的最高价氧化物对应的水化物的化学式为H3RO4,则X的最高正价为+5价,最高正化合价-8=最低负价,最低化合价为5-8=-3价,
故选:C.
点评 本题考查元素在周期表中的位置以及元素的性质,题目难度不大,注意最高化合价与最低化合价之间的关系,二者绝对值之和为8.

练习册系列答案
 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
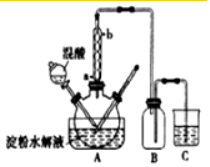
7.下列实验装置或操作能达到实验目的是( )


| A. | 制取Fe(OH)2的装置及操作 | |
| B. | 某溶液用盐酸酸化后再滴加硝酸钡溶液,检验溶液中是否含有SO42- | |
| C. | 向滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后溶液的红色褪去,可证明Na2CO3溶液显碱性是由于CO32-水解造成的 | |
| D. | 将氯化铁饱和滚液与稀氨水混合,加热至沸腾,制备Fe(OH)3胶体 |
8.常温下,有甲、乙两份体积为1L,浓度均为0.1mol•L-1的醋酸溶液,其pH为3,①甲用蒸馏水稀释100倍后,溶液的pH变为x;②乙与等体积、浓度为0.2mol•L-1的NaOH混合,在混合液中:n(CH3COO-)+n(OH-)-n(H+)=y mol,x、y的正确答案组合为( )
| A. | 5; 0.1 | B. | 5; 0.2 | C. | 3<x<5; 0.1 | D. | 3<x<5; 0.2 |
12.完成下列实验所需选择的装置或仪器都正确的是( )
| A | B | C | D | |
| 实验 | 分离汽油和水 | 通过蒸馏乙醇的水溶 液获得无水乙醇 | 分离 CCl4 中的 I2 | 除去 CO2 气体中的 HCl 气体 |
| 装 置 或 仪 器 | 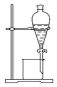 | 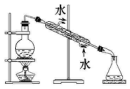 | 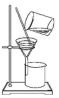 | 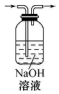 |
| A. | A | B. | B | C. | C | D. | D |
2.实验室里由粗盐制备精盐的实验中,必需的操作步骤有( )
| A. | 分液 | B. | 过滤 | C. | 溶解 | D. | 蒸发结晶 |
6.如图表示吸热反应、置换反应、氧化还原反应之间的关系,下列反应中,属于Ⅴ区域的是( )
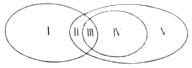

| A. | NaOH+HCl═NaCl+H2O | B. | 2Na2O2+2H2O═4NaOH+O2↑ | ||
| C. | 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑ | D. | 2Na+2H2O═2NaOH+H2↑ |
16.下列实验方案的设计中,可行的是( )
| A. | 加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铝粉 | |
| B. | 用萃取的方法分离煤油和汽油 | |
| C. | 用溶解、过滤的方法分离KNO3和NaCl固体的混合物 | |
| D. | 向某溶液中先加BaCl2溶液,若有白色沉淀,再加稀盐酸,沉淀不溶解,可检验其中含有SO${\;}_{4}^{2-}$ |
 .
.