题目内容
3.设NA为阿伏加德罗常数的值,下列关于0.2 mol•L-1Ba(NO3)2溶液的说法不正确的是( )| A. | 1 L溶液中含Ba2+、N${O}_{3}^{-}$的总数是0.6NA | |
| B. | 500 mL溶液中Ba2+的浓度是0.2 mol•L-1 | |
| C. | 500 mL溶液中N${O}_{3}^{-}$的浓度是0.2 mol•L-1 | |
| D. | 1 L溶液中含有0.4NA个N${O}_{3}^{-}$ |
分析 依据n=CV计算硝酸钡的物质的量,结合硝酸钡电离生成钡离子和硝酸根离子,溶液具有均一性,据此解答.
解答 解:A.1 L0.2 mol•L-1Ba(NO3)2溶液含有硝酸钡物质的量为1L×0.2mol/L=0.2mol,含有钡离子0.2mol,含有硝酸根离子0.4mol,含Ba2+、NO3-的总数是0.6NA,故A正确;
B.0.2 mol•L-1Ba(NO3)2溶液中钡离子浓度为0.2mol/L,溶液具有均一性,与体积无关,所以500 mL溶液中Ba2+的浓度是0.2 mol•L-1,故B正确;
C.1mol硝酸钡含有2mol 硝酸根离子,0.2 mol•L-1Ba(NO3)2溶液,硝酸根离子浓度为0.4mol/L,故C错误;
D.0.2 mol•L-1Ba(NO3)2溶液,硝酸根离子浓度为0.4mol/L,1 L溶液中含有0.4NA个NO3-,故D正确;
故选:C.
点评 本题考查了有关物质的量浓度计算,明确物质的量浓度定义及硝酸钡结构是解题关键,题目难度不大,注意溶液的均一性.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
13.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 在1 L 2 mol•L-1的硝酸镁溶液中含有的硝酸根离子数为2NA | |
| B. | 2.3 g Na变成Na+时失去的电子数目为0.2NA | |
| C. | 1 mol H2O的质量与NA个H2O的质量之和相等 | |
| D. | 在通常状况下,22.4 L O2与N2的混合物所含分子数为NA |
14.有机物CH2=CHCH2CH(OH)COOH在不同条件下至少可能发生7种不同类型的反应:①取代 ②加成 ③消去 ④氧化 ⑤酯化 ⑥缩聚 ⑦加聚,其中可能由于分子结构中含有“-OH”而发生的反应( )
| A. | ①③⑤⑦ | B. | ②④⑥⑦ | C. | ②③④⑤ | D. | ①③④⑤⑥ |
11.化学中常借助曲线图来表示某种变化过程,如:①平衡移动过程 ②中和滴定过程 ③沉淀的生成和溶解过程 ④固体物质的溶解度变化过程.下列曲线图中从左到右依次表示上述过程的正确顺序是( )
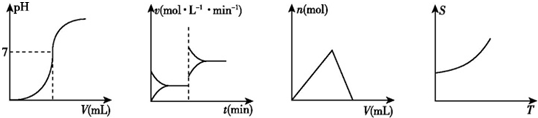

| A. | ①②③④ | B. | ②①③④ | C. | ③②②① | D. | ②③①④ |
18.四种短周期元素W、X、Y、Z,原子序数依次增大,请结合表中信息回答下列问题.
(1)Z在元素周期表中位于ⅣA族.
(2)上述元素的最高价氧化物对应的水化物中,有一种物质在一定条件下均能与其他三种物质发生化学反应,该元素是Na(填元素符号).
(3)①下列可作为比较X和Y金属性强弱的依据是bc(填序号).
a.自然界中的含量
b.相应氯化物水溶液的pH
c.单质与水反应的难易程度
d.单质与酸反应时失去的电子数
②从原子结构的角度解释X的金属性强于Y的原因:电子层相同,核电荷数Al>Na,原子半径Na>Al,所以原子核对最外层电子的吸引力Na<Al,失电子能力Na>Al.
(4)W的一种氢化物HW3可用于有机合成,其酸性与醋酸相似.体积和浓度均相等的HW3与X的最高价氧化物对应的水化物的溶液混合,反应的化学方程式是HN3+NaOH═NaN3+H2O,混合后溶液中离子浓度由大到小的顺序是c(Na+)>c(N3-)>c(OH-)>c(H+).
(5)Y单质和Mg组成的混合物是一种焰火原料,某兴趣小组设计如下所示的实验方案,测定混合物中Y的质量分数.
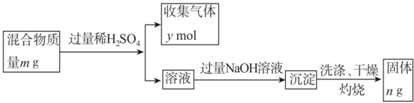
能确定混合物中Y的质量分数的数据有abc(填序号).
a.m、n b.m、y c.n、y.
| W | X | Y | Z | |
| 结构或性质 | 最高价氧化物对应的水化物与其气态氢化物反应得到离子化合物 | 焰色反应呈黄色 | 在同周期主族元素形成的简单离子中,离子半径最小 | 最高正价与最低负价之和为零 |
(2)上述元素的最高价氧化物对应的水化物中,有一种物质在一定条件下均能与其他三种物质发生化学反应,该元素是Na(填元素符号).
(3)①下列可作为比较X和Y金属性强弱的依据是bc(填序号).
a.自然界中的含量
b.相应氯化物水溶液的pH
c.单质与水反应的难易程度
d.单质与酸反应时失去的电子数
②从原子结构的角度解释X的金属性强于Y的原因:电子层相同,核电荷数Al>Na,原子半径Na>Al,所以原子核对最外层电子的吸引力Na<Al,失电子能力Na>Al.
(4)W的一种氢化物HW3可用于有机合成,其酸性与醋酸相似.体积和浓度均相等的HW3与X的最高价氧化物对应的水化物的溶液混合,反应的化学方程式是HN3+NaOH═NaN3+H2O,混合后溶液中离子浓度由大到小的顺序是c(Na+)>c(N3-)>c(OH-)>c(H+).
(5)Y单质和Mg组成的混合物是一种焰火原料,某兴趣小组设计如下所示的实验方案,测定混合物中Y的质量分数.

能确定混合物中Y的质量分数的数据有abc(填序号).
a.m、n b.m、y c.n、y.
15.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 0.1molNa与O2在一定条件下生成Na2O和Na2O2混合物时,失去电子数为0.2NA | |
| B. | 50mL 12mol•L-1浓盐酸与足量二氧化锰加热反应,生成Cl2的分子数为0.15NA | |
| C. | 常温下,100mL 1mol•L-1Na2CO3溶液中阴离子总数等于0.1NA | |
| D. | 标准状况下,6.72LCO2中所含的共用电子对数为1.2NA |
8.下列关于化合物的式量(M)叙述不正确的是( )
| A. | 式量为30的碳、氢、氧组成的化合物无同分异构体 | |
| B. | 式量为128的烃的分子式不一定是C9H20 | |
| C. | 烃的式量可以是偶数,也可以是奇数 | |
| D. | 有机物分子中,H原子数可以是偶数,也可以是奇数 |
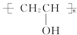 $\stackrel{H+}{→}$
$\stackrel{H+}{→}$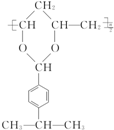
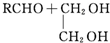 $\stackrel{H+}{→}$
$\stackrel{H+}{→}$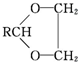 +H2O
+H2O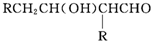 $→_{-H_{2}O}^{△}$
$→_{-H_{2}O}^{△}$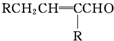
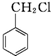 $\stackrel{K_{2}Cr_{2}O_{7}-KOH}{→}$
$\stackrel{K_{2}Cr_{2}O_{7}-KOH}{→}$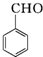
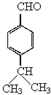 ,E中含有的官能团名称为羟基、醛基.
,E中含有的官能团名称为羟基、醛基.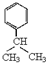 .
.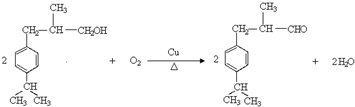 .
. .
.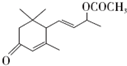 是否互为同分异构体否(填“是”或“否”),符合下列条件的
是否互为同分异构体否(填“是”或“否”),符合下列条件的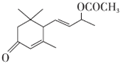 的同分异构体有2种,写出其中一种的结构简式
的同分异构体有2种,写出其中一种的结构简式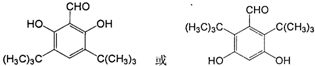 .
.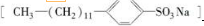 是常用洗涤剂的主要成分.
是常用洗涤剂的主要成分.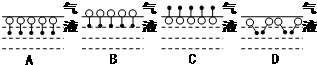
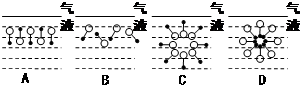
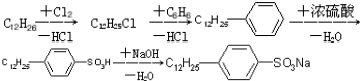
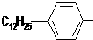 .
.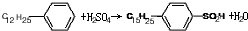 ,反应类型为取代反应.
,反应类型为取代反应.