题目内容
3.甲、乙、丙、丁四种物质之间的转化关系如图所示,则下列说法错误的是( )
| A. | 若甲是C,则乙可能是O2 | B. | 若甲是Fe,则乙可能是Cl2 | ||
| C. | 若甲是NaOH溶液,则乙可能是SO2 | D. | 若甲是H2S,则乙可能是O2 |
分析 A.若甲是C,乙是O2,丙为CO,丁为二氧化碳,二氧化碳与碳反应得到CO;
B.若甲是Fe,乙是Cl2,则丙为氯化铁,氯化铁与氯气不反应;
C.若甲是NaOH溶液,乙是SO2,丙为亚硫酸钠,丁为亚硫酸氢钠,氢氧化钠与亚硫酸氢钠反应生成硫化钠;
D.若甲是H2S,乙是O2,丙为硫,丁为二氧化硫,二氧化硫与硫化氢反应得到硫.
解答 解:A.若甲是C,乙是O2,丙为CO,丁为二氧化碳,二氧化碳与碳反应得到CO,符合转化关系,故A正确;
B.若甲是Fe,乙是Cl2,则丙为氯化铁,氯化铁与氯气不反应,不符合转化关系,故B错误;
C.若甲是NaOH溶液,乙是SO2,丙为亚硫酸钠,丁为亚硫酸氢钠,氢氧化钠与亚硫酸氢钠反应生成硫化钠,符合转化关系,故C正确;
D.若甲是H2S,乙是O2,丙为硫,丁为二氧化硫,二氧化硫与硫化氢反应得到硫,符合转化关系,故D正确.
故选:B.
点评 本题考查无机物推断,需要学生熟练掌握元素化合物性质,熟练掌握中学常见连续反应.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.天然气脱硫的方法有多种,一种是干法脱硫,其涉及的反应:H2(g)+CO(g)+SO2(g)?H2O(g)+CO2(g)+S(s)+Q(Q>0).要提高脱硫率可采取的措施是( )
| A. | 加催化剂 | B. | 分离出硫 | C. | 减压 | D. | 加生石灰 |
18.从矿物学资料查得,当胆矾溶液渗人地下,遇黄铁矿(FeS2)时可生成辉铜矿(Cu2S),同时还生成FeSO4和H2SO4,下列有关叙述中正确的是( )
| A. | 在反应中,FeS2是氧化剂,不是还原剂 | |
| B. | 在反应中,CuSO4是氧化剂,FeS2是还原剂 | |
| C. | 反应中Cu2+与FeS2的物质的量之比是14:5 | |
| D. | 反应中每生成1mol Cu2S共得2mol电子 |
11.常温下,0.05mol•L-1Ba(OH)2溶液的pH为( )
| A. | 13 | B. | 1 | C. | 1.3 | D. | 12.7 |
8.下表是元素周期表中短周期元素的一部分,表中所列字母分别代表一种元素.
(1)上述元素的单质中熔点最高的可能是石墨(填名称).
(2)D的氢化物比G的氢化物稳定,其原因是D的非金属性比G的强的缘故.
(3)在一定条件下,A与E可形成一种极易溶于水的气态化合物,该物质溶于水后的溶液呈碱性(填“酸”、“碱”或“中”),用电子式表示该物质的形成过程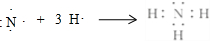 .
.
(4)“神舟”六号载人飞船内需要有一种化合物来吸收航天员呼出的CO2,你认为该物质应该是由上表中的C、F(填字母序号)元素组成的,用化学方程式表示吸收原理:2Na2O2+2CO2=2Na2CO3+O2
(5)飞船中需要制造一种适合航天员生存的人工态环境,还应该在氧气中充入一种稀释气体,该气体化学式为N2,其电子式为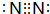 .
.
| A | B | ||||||
| D | E | F | |||||
| C | G | H |
(2)D的氢化物比G的氢化物稳定,其原因是D的非金属性比G的强的缘故.
(3)在一定条件下,A与E可形成一种极易溶于水的气态化合物,该物质溶于水后的溶液呈碱性(填“酸”、“碱”或“中”),用电子式表示该物质的形成过程
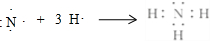 .
.(4)“神舟”六号载人飞船内需要有一种化合物来吸收航天员呼出的CO2,你认为该物质应该是由上表中的C、F(填字母序号)元素组成的,用化学方程式表示吸收原理:2Na2O2+2CO2=2Na2CO3+O2
(5)飞船中需要制造一种适合航天员生存的人工态环境,还应该在氧气中充入一种稀释气体,该气体化学式为N2,其电子式为
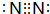 .
.
15.乙醛(CH3CHO)、乙酸、乙酸乙酯三种有机物按一定比例组成的混合物中,若含氧的质量分数为A%,则此混合物中含氢的质量分数为( )
| A. | $\frac{6A%}{7}$ | B. | $\frac{1-A%}{7}$ | C. | $\frac{6(1-A%)}{7}$ | D. | (100-$\frac{7A}{6}$)% |
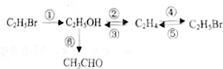
 ②CH3CH2OH
②CH3CH2OH CH2=CH2↑+H2O
CH2=CH2↑+H2O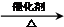 CH3CH2Br 乙醛的银镜反应
CH3CH2Br 乙醛的银镜反应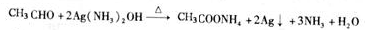
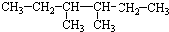 .
.