题目内容
X、Y、Z和W代表原子序数依次增大的四种短周期主族元素,它们满足以下条件:①元素周期表中,Z与Y相邻,Z与W也相邻;②Y、Z和W三种元素的原子最外层电子数之和为17.请填空(用元素符号或化学用语):
(1)Y是 ,Z是 ,W是 ;
(2)Y元素的最高价氧化物的化学式是 ,其对应的水化物分子式是 ;
(3)X、Y、Z和W可组成一化合物,其原子个数之比为8:2:4:1.该化合物的化学式 ,其中存在的化学键类型有 ;
(4)上述四种元素中,非金属性最强的是 ,非金属性最弱的是 .
(1)Y是
(2)Y元素的最高价氧化物的化学式是
(3)X、Y、Z和W可组成一化合物,其原子个数之比为8:2:4:1.该化合物的化学式
(4)上述四种元素中,非金属性最强的是
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:若Y、Z、W三者处于同一周期或同一主族,最外层电子数之和不可能为17,处于不同周期的Y、Z、W两两相邻,可能出现的位置关系有:
 、
、
设Y的最外层电子数为x,若为第一种情况,则有x+x+1+x+1=17,解得x=5,Y、Z、W对应的三种元素分别为N,O,S;若为第二种情况,则有x+x+x+1=17,x为分数,不合理,由于Y是N元素,那么X只能是位于其前面的H、He、Li、Be、B五种元素,X、Y、Z和W可组成一化合物,其原子个数之比为8:2:4:1,化合物中硫原子与氧原子个数之比为1:4,为硫酸根,化合物中x原子与氮原子个数之比为4:1,且x的原子序数比氮原子小,则X为H,X与N形成铵根离子,结合对应单质化合物的性质解答该题.
 、
、
设Y的最外层电子数为x,若为第一种情况,则有x+x+1+x+1=17,解得x=5,Y、Z、W对应的三种元素分别为N,O,S;若为第二种情况,则有x+x+x+1=17,x为分数,不合理,由于Y是N元素,那么X只能是位于其前面的H、He、Li、Be、B五种元素,X、Y、Z和W可组成一化合物,其原子个数之比为8:2:4:1,化合物中硫原子与氧原子个数之比为1:4,为硫酸根,化合物中x原子与氮原子个数之比为4:1,且x的原子序数比氮原子小,则X为H,X与N形成铵根离子,结合对应单质化合物的性质解答该题.
解答:
解:(1)若Y、Z、W三者处于同一周期或同一主族,最外层电子数之和不可能为17,处于不同周期的Y、Z、W两两相邻,可能出现的位置关系有:
 、
、
设Y的最外层电子数为x,若为第一种情况,则有x+x+1+x+1=17,解得x=5,Y、Z、W对应的三种元素分别为N,O,S;若为第二种情况,则有x+x+x+1=17,x为分数,不合理,由于Y是N元素,那么X只能是位于其前面的H、He、Li、Be、B五种元素,X、Y、Z和W可组成一化合物,其原子个数之比为8:2:4:1,化合物中硫原子与氧原子个数之比为1:4,为硫酸根,化合物中x原子与氮原子个数之比为4:1,且x的原子序数比氮原子小,则X为H,X与N形成铵根离子,
故答案为:N;O;S;
(2)Y为N,Y元素的最高价氧化物的化学式是N2O5,其对应的水化物分子式是HNO3,
故答案为:N2O5;HNO3;
(3)化合物中硫原子与氧原子个数之比为1:4,为硫酸根,化合物中x原子与氮原子个数之比为4:1,且x的原子序数比氮原子小,则X为H,X与N形成铵根离子,所以该化合物为硫酸铵,其化学式为(NH4)2SO4,其中存在的化学键类型有离子键和共价键,
故答案为:(NH4)2SO4;离子键和共价键;
(4)根据元素周期律,在N、O、S、H中,非金属性最强的是O,非金属性最弱的是H,
故答案为:O;H;
 、
、
设Y的最外层电子数为x,若为第一种情况,则有x+x+1+x+1=17,解得x=5,Y、Z、W对应的三种元素分别为N,O,S;若为第二种情况,则有x+x+x+1=17,x为分数,不合理,由于Y是N元素,那么X只能是位于其前面的H、He、Li、Be、B五种元素,X、Y、Z和W可组成一化合物,其原子个数之比为8:2:4:1,化合物中硫原子与氧原子个数之比为1:4,为硫酸根,化合物中x原子与氮原子个数之比为4:1,且x的原子序数比氮原子小,则X为H,X与N形成铵根离子,
故答案为:N;O;S;
(2)Y为N,Y元素的最高价氧化物的化学式是N2O5,其对应的水化物分子式是HNO3,
故答案为:N2O5;HNO3;
(3)化合物中硫原子与氧原子个数之比为1:4,为硫酸根,化合物中x原子与氮原子个数之比为4:1,且x的原子序数比氮原子小,则X为H,X与N形成铵根离子,所以该化合物为硫酸铵,其化学式为(NH4)2SO4,其中存在的化学键类型有离子键和共价键,
故答案为:(NH4)2SO4;离子键和共价键;
(4)根据元素周期律,在N、O、S、H中,非金属性最强的是O,非金属性最弱的是H,
故答案为:O;H;
点评:本题考查学生对元素结构与位置性质关系的利用,难度不大,关键在确定元素Y、Z、W的可能位置,利用最外层电子数之和为17推断.

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
下列溶液中粒子的物质的量浓度关系一定正确的是( )
| A、常温下,pH=9的NaHA溶液:c(Na+)>c(HA-)>c(A2-)>c(H2A) |
| B、Na2CO3溶液:c(H+)-c(OH-)=c(HC03-)+2c(CO32-)-c(Na+) |
| C、向NaOH溶液中滴入CH3COOH溶液后溶液显碱性:c(CH3COO-)>c(OH-)>c(H+) |
| D、浓度均为0.1mol?L-1的HF溶液与KF溶液等体积混合:c(F-)+c(HF)=0.2mol?L-1 |

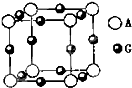 已知:A、B、C、D、E、F、G七种元素的核电荷数依次增大,属于元素周期表中前四周期的元素.其中A原子在基态时p轨道半充满且电负性是同族元素中最大的;D、E原子核外的M层中均有两个未成对电子;G原子核外最外层电子数与B相同,其余各层均充满.B、E两元素组成化合物B2E的晶体为离子晶体.C、F的原子均有三个能层,C原子的第一至第四电离能(kJ/mol)分别为:578、1817、2745、ll575;C与F能形成原子数目比为1:3、熔点为190℃的化合物Q.
已知:A、B、C、D、E、F、G七种元素的核电荷数依次增大,属于元素周期表中前四周期的元素.其中A原子在基态时p轨道半充满且电负性是同族元素中最大的;D、E原子核外的M层中均有两个未成对电子;G原子核外最外层电子数与B相同,其余各层均充满.B、E两元素组成化合物B2E的晶体为离子晶体.C、F的原子均有三个能层,C原子的第一至第四电离能(kJ/mol)分别为:578、1817、2745、ll575;C与F能形成原子数目比为1:3、熔点为190℃的化合物Q. 在硬质玻璃管中的A,B,C处依次放有浸有KBr溶液、KI溶液、淀粉溶液的三个棉球(如图所示).向左端导入Cl2,在B处加热,可观察到A处棉球呈
在硬质玻璃管中的A,B,C处依次放有浸有KBr溶液、KI溶液、淀粉溶液的三个棉球(如图所示).向左端导入Cl2,在B处加热,可观察到A处棉球呈