题目内容
3.某有机物在氧气中充分燃烧生成的水和二氧化碳的物质的量比为1:1,由此可得出结论是( )| A. | 该有机物分子中碳、氢、氧原子个数比为1:2:3 | |
| B. | 该有机物分子中碳、氢原子个数比为1:2 | |
| C. | 该有机物中必含氧元素 | |
| D. | 该有机物中可能不含氧元素 |
分析 因生成CO2和H2O的物质的量比为1:1,则n(C):n(H)=1:(1×2)=1:2,题干信息无法判断有机物分子中是否含有氧元素,以此解答该题.
解答 解:A.只根据生成产物为二氧化碳和水,无法判断该有机物中是否含有氧原子,故A错误;
B.生成CO2和H2O的物质的量比为1:1,则n(C):n(H)=1:(1×2)=1:2,故B正确;
C.该有机物充分燃烧生成二氧化碳和水,其分子中可能含有氧原子,故C错误;
D.题干信息无法确定该有机物分子中是否含有氧原子,故D正确;
故选BD.
点评 本题考查了有机物结构与性质、有机物分子式的确定,题目难度不大,注意明确常见有机物组成、结构与性质,明确确定有机物分子式的方法.

练习册系列答案
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
13.已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]-,铬的化合物有毒,由于+6价铬的强氧化性,其毒性是+3价铬毒性的100倍.因此,必须对含铬的废水进行处理,可采用以下两种方法.
★还原法:在酸性介质中用FeSO4等将+6价铬还原成+3价铬.
具体流程如下:

有关离子完全沉淀的pH如表:
(1)写出Cr2O72-与FeSO4溶液在酸性条件下反应的离子方程式Cr2O72-+6Fe2++14H+═2 Cr3++6Fe3++7H2O.
(2)还原+6价铬还可选用以下的BD试剂(填序号).
A.明矾 B.铁屑 C.生石灰 D.亚硫酸氢钠
(3)在含铬废水中加入FeSO4,再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀.则在操作②中可用于调节溶液pH的试剂为:CD(填序号);
A.Na2O2 B.Ba(OH)2 C.Ca(OH)2 D.NaOH
此时调节溶液的pH范围在B(填序号)最佳.
A.3~4 B.6~8 C.10~11 D.12~14
★电解法:将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解.阳极区生成的Fe2+和Cr2O${\;}_{7}^{2-}$发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3和Cr(OH)3沉淀除去.
(4)写出阴极的电极反应式2H++2e-═H2↑或2H2O+2e-═H2↑+2OH-;.
(5)电解法中加入氯化钠的作用是:增强溶液导电性.
★还原法:在酸性介质中用FeSO4等将+6价铬还原成+3价铬.
具体流程如下:

有关离子完全沉淀的pH如表:
| 有关离子 | Fe2+ | Fe3+ | Cr3+ |
| 完全沉淀为对应氢氧化物的pH | 9.0 | 3.2 | 5.6 |
(2)还原+6价铬还可选用以下的BD试剂(填序号).
A.明矾 B.铁屑 C.生石灰 D.亚硫酸氢钠
(3)在含铬废水中加入FeSO4,再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀.则在操作②中可用于调节溶液pH的试剂为:CD(填序号);
A.Na2O2 B.Ba(OH)2 C.Ca(OH)2 D.NaOH
此时调节溶液的pH范围在B(填序号)最佳.
A.3~4 B.6~8 C.10~11 D.12~14
★电解法:将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解.阳极区生成的Fe2+和Cr2O${\;}_{7}^{2-}$发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3和Cr(OH)3沉淀除去.
(4)写出阴极的电极反应式2H++2e-═H2↑或2H2O+2e-═H2↑+2OH-;.
(5)电解法中加入氯化钠的作用是:增强溶液导电性.
14.某学生做元素性质递变实验时自己设计了一套方案,并记录了有关实验现象如下表(实验方案与实验现象没对应)
请你帮助该同学完成实验报告:
(1)实验的目的验证第三周期金属元素的金属性的递变规律;
(2)实验内容:与实验方案1-5对应的实验现象依次为E、A、C、B、D(填:字母编号);实验现象(A)为:钠浮在水面上,熔化化成小球,四处游动,发出嘶嘶响声,溶液变红;
(3)实验结论同周期从左到右元素的金属性逐渐减弱.
| 实验现象 |
| (A) |
| (B)反应不十分强烈,产生的气体可在空气中燃烧 |
| (C)剧烈反应,产生可燃性气体 |
| (D)生成白色胶状沉淀,然后沉淀消失 |
| (E)产生气体,可在空气中燃烧,溶液变成浅红色 |
| 实验方案 |
| 1.用砂纸打磨后的镁带加适量水加热,再向反应后溶液中滴加酚酞 |
| 2.钠与滴有酚酞的试液的冷水反应 |
| 3.镁带与2mol/L的盐酸反应 |
| 4.铝条与2mol/L的盐酸反应 |
| 5.向氯化铝溶液中滴加氢氧化钠溶液至过量 |
(1)实验的目的验证第三周期金属元素的金属性的递变规律;
(2)实验内容:与实验方案1-5对应的实验现象依次为E、A、C、B、D(填:字母编号);实验现象(A)为:钠浮在水面上,熔化化成小球,四处游动,发出嘶嘶响声,溶液变红;
(3)实验结论同周期从左到右元素的金属性逐渐减弱.
11.下列高聚物经简单处理可以从线型结构变成体型结构的是( )
①
②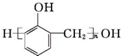
③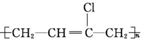
④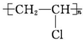
①

②

③
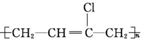
④
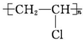
| A. | ①② | B. | ③④ | C. | ①④ | D. | ②③ |
18.下列物质属于离子化合物的是( )
| A. | CO2 | B. | H2O | C. | NaOH | D. | H2SO4 |
19.在标准状况下将19.2g铜粉投入一定量浓HNO3中随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后共收集到由NO2和NO组成的混和气体8.96L,则混和气体中NO的体积为( )
| A. | 2240mL | B. | 1008mL | C. | 3360mL | D. | 448mL |