题目内容
11.根据下表信息,判断以下叙述正确的是( )部分短周期元素的原子半径及主要化合价
| 元素代号 | G | L | M | Q | R | T |
| 原子半径/nm | 0.186 | 0.160 | 0.143 | 0.104 | 0.075 | 0.066 |
| 主要化合价 | +1 | +2 | +3 | +6、-2 | +5、-3 | -2 |
| A. | 单质的还原性:G<L<M | B. | 非金属性:T<Q | ||
| C. | 气态氢化物的稳定性:R>T | D. | L2+与T2-的核外电子数相等 |
分析 短周期元素,由元素的化合价可知,T只有-2价,则T为O元素,Q有+6、-2价,可知Q为S元素;R有+5、-3价,则R为氮元素;G、L、M只有正化合价,原子半径G>L>M,则G为Na元素,L为Mg,M为Al元素.
A、A金属性越强,单质的还原性越强,同周期自左而右金属性减弱;
B、同主族从上往下非金属性减弱;
C、非金属性越强氢化物越稳定;
D、L、T的离子电子层排布相同.
解答 解:A、同周期自左而右金属性减弱,所以G>L>M,故A错误;
B、同主族从上往下非金属性减弱,所以T>Q,故B错误;
C、R为氮元素,T为O元素的,非金属性:O>N,所以气态氢化物的稳定性:R<T,故C错误;
D、L、T的离子电子层排布相同,L2+与T2-的核外电子数相等,都是10个电子,故D正确;
故选D.
点评 本题考查元素的性质与位置关系,学生能利用原子半径及化合价来推断出元素是解答本题的关键,并熟悉元素及其单质、化合物的性质来解答即可,难度不大.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
1.下列说法正确的是( )
| A. | 乙烯、聚乙烯、乙炔、聚乙炔都能使溴水或高锰酸钾溶液褪色,但与两种试剂发生反应的反应类型是不同的 | |
| B. | 最简单的芳香族化合物是苯,最简单的糖是葡萄糖 | |
| C. | 常温下苯与液溴、铁粉混合反应生成的油状有机物呈红褐色,这是溶有氢氧化铁杂质造成的 | |
| D. | 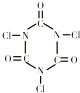 三氯异氰尿酸(TCCA)是用于游泳池等公共场合消毒的第三代产品,具有强烈的氯气刺激味,含有效氯在90%以上,结构简式如图所示.据此推测TCCA分子中氯元素显正价 |
2.下列措施肯定能使反应速率增大的是( )
| A. | 增大反应物的量 | B. | 增大压强 | C. | 适当升高温度 | D. | 使用催化剂 |
16.下列各组有机物,不管它们以何种比例混合,只要混合物的总质量一定,则完全燃烧时,所产生的二氧化碳的质量也不变的是( )
| A. | CH4和C2H6 | B. | C2H4和C3H6 | C. | C2H6和C3H6 | D. | C2H4和C3H4 |
3.属于天然高分子化合物的组合是( )
| A. | 聚乙烯、淀粉 | B. | 油脂、蛋白质 | C. | 酚醛树脂、纤维素 | D. | 纤维素、淀粉 |
1.某实验小组对H2O2的分解做了如下探究.下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将质量相同的粉末状和块状的MnO2分别加入盛有15ml 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
(1)写出上述实验中发生反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)实验结果表明,催化剂的催化效果与催化剂的表面积有关.
| MnO2 | 触摸试管情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 3.5min |
| 块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30min |
(2)实验结果表明,催化剂的催化效果与催化剂的表面积有关.
 在银锌原电池中,以硫酸铜为电解质溶液,锌为负极,电极上发生的是(“氧化”或“还原”)氧化反应,银电极上的电极反应式为Cu2++2e-═Cu.
在银锌原电池中,以硫酸铜为电解质溶液,锌为负极,电极上发生的是(“氧化”或“还原”)氧化反应,银电极上的电极反应式为Cu2++2e-═Cu.
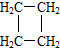 可简写成
可简写成 )
)
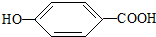 ),其反应方程式为:
),其反应方程式为: 、
、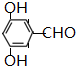 .
.