题目内容
化合物YX2、ZX2中X、Y、Z都是前三周期元素,X与Y同周期,Y与Z同主族,Y元素原子最外层的p轨道中的电子数等于前一电子层的电子总数,X原子最外层的p轨道中有一个轨道填充了2个电子.
(1)X原子的电子排布式是 ,Y原子的价层电子排布图是: .
(2)YX2的分子构型是 ,YX2的熔、沸点比ZX2 (填“高”或“低”).
(3)YX2分子中,Y原子的杂化类型是 ,YX2分子中含 个π键.
(4)如图表示一些晶体的结构(晶胞),其中代表YX2的是 ,代表ZX2的是 (填序号,下同).

(1)X原子的电子排布式是
(2)YX2的分子构型是
(3)YX2分子中,Y原子的杂化类型是
(4)如图表示一些晶体的结构(晶胞),其中代表YX2的是

考点:位置结构性质的相互关系应用,原子轨道杂化方式及杂化类型判断
专题:
分析:化合物YX2、ZX2中X、Y、Z都是前三周期元素,X原子最外能层的p能级中有一个轨道填充了2个电子,则X的最外层电子排布式为ns2np4,为第VIA族元素;
Y原子的最外层中p能级的电子数等于前一能层电子总数,p能级最多排列6个电子,则Y次外层为K层,Y原子最外层p能级上电子数是2,Y原子含有6个电子,为C元素,XX与Y同周期,Y与Z同主族,所以X是O元素,Z为Si元素,然后结合元素化合物性质、物质的结构来分析解答.
Y原子的最外层中p能级的电子数等于前一能层电子总数,p能级最多排列6个电子,则Y次外层为K层,Y原子最外层p能级上电子数是2,Y原子含有6个电子,为C元素,XX与Y同周期,Y与Z同主族,所以X是O元素,Z为Si元素,然后结合元素化合物性质、物质的结构来分析解答.
解答:
解:化合物YX2、ZX2中X、Y、Z都是前三周期元素,X原子最外能层的p能级中有一个轨道填充了2个电子,则X的最外层电子排布式为ns2np4,为第VIA族元素;
Y原子的最外层中p能级的电子数等于前一能层电子总数,p能级最多排列6个电子,则Y次外层为K层,Y原子最外层p能级上电子数是2,Y原子含有6个电子,为C元素,XX与Y同周期,Y与Z同主族,所以X是O元素,Z为Si元素,
(1)X是O元素,原子序数为8,其最外层有6个电子,所以O的电子排布式为1s22s22p4,Y是C原子,根据构造原理知,其核外电子排布式为:1s22s22p2,Y原子的价电子轨道表示式为 故答案为:1s22s22p2;
故答案为:1s22s22p2;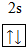
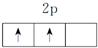 ;
;
(2)YX2的结构式为O=C=O,C为sp杂化,分子构型为直线型,因CO2为分子晶体,SiO2为原子晶体,则二氧化碳熔、沸点低,
故答案为:直线型;低;
(3)YX2分子中,结构式为O=C=O及直线结构可知,由Y原子的杂化类型是sp杂化,双键中有1个π键,则一个YX2分子中含2个π键,故答案为:sp杂化;2;
(4)XY2是CO2,图象B符合,ZY2是SiO2,图C符合,故答案为:B;C.
Y原子的最外层中p能级的电子数等于前一能层电子总数,p能级最多排列6个电子,则Y次外层为K层,Y原子最外层p能级上电子数是2,Y原子含有6个电子,为C元素,XX与Y同周期,Y与Z同主族,所以X是O元素,Z为Si元素,
(1)X是O元素,原子序数为8,其最外层有6个电子,所以O的电子排布式为1s22s22p4,Y是C原子,根据构造原理知,其核外电子排布式为:1s22s22p2,Y原子的价电子轨道表示式为
 故答案为:1s22s22p2;
故答案为:1s22s22p2;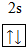
 ;
;(2)YX2的结构式为O=C=O,C为sp杂化,分子构型为直线型,因CO2为分子晶体,SiO2为原子晶体,则二氧化碳熔、沸点低,
故答案为:直线型;低;
(3)YX2分子中,结构式为O=C=O及直线结构可知,由Y原子的杂化类型是sp杂化,双键中有1个π键,则一个YX2分子中含2个π键,故答案为:sp杂化;2;
(4)XY2是CO2,图象B符合,ZY2是SiO2,图C符合,故答案为:B;C.
点评:本题考查位置、结构、性质的关系及应用,为高频考点,把握原子中电子排布及分子结构为解答的关键,侧重分析、推断能力的考查,题目难度不大.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
某有机物是药物生产的中间体,其结构简式如右图.下列有关叙述不正确的是( )


| A、该有机物与浓溴水可发生取代反应 |
| B、1 mol该有机物与足量NaOH溶液反应最多消耗4 mol NaOH |
| C、该有机物与浓硫酸混合共热可发生消去反应 |
| D、该有机物经催化氧化后与新制氢氧化铜悬浊液共热生成砖红色沉淀 |
从金属利用的历史看,先是青铜器时代,而后是铁器时代,铝的冶炼是近百年的事.决定金属使用年代先后顺序的关键因素是( )
| A、金属的活动性 |
| B、金属的导电性 |
| C、金属的延展性 |
| D、地壳中金属元素的含量 |
 甲、乙、丙、丁、戊五种元素,其中甲元素原子核外L层上s能级和p能级电子个数相同;乙元素原子3p能级上只有1对成对电子;丙和丁元素原子N层上都只有1个电子,但其中丙元素原子各内层均已充满;而丁元素原子次外层的电子充满在2个能级中;戊元素单质常温时为气态,原子最外层电子排布图如图所示:试回答以下问题.
甲、乙、丙、丁、戊五种元素,其中甲元素原子核外L层上s能级和p能级电子个数相同;乙元素原子3p能级上只有1对成对电子;丙和丁元素原子N层上都只有1个电子,但其中丙元素原子各内层均已充满;而丁元素原子次外层的电子充满在2个能级中;戊元素单质常温时为气态,原子最外层电子排布图如图所示:试回答以下问题.