题目内容
19.设NA表示阿伏伽德罗常数的值,下列说法不正确的是( )| A. | 4.0g 氦气中含有的最外层电子数为4NA | |
| B. | 3.9g 2H37Cl中含有的中子数为2.1NA | |
| C. | 标准状况下,11.2L丙烷中含有的非极性键数目为NA | |
| D. | 100mL 1mol•L-1 CH3COOH溶液中含有的分子数目大于0.1NA |
分析 A.稀有气体为单原子分子,氦原子最外层含有2个电子;
B.2H37Cl中含有21个中子,其摩尔质量为39g/mol;
C.丙烷分子中含有2个碳碳非极性键,0.5mol丙烷分子中含有1mol非极性键;
D.醋酸溶液中含有醋酸和水分子.
解答 解:A.4.0g 氦气的物质的量为:$\frac{4.0g}{4g/mol}$=1mol,1mol氦气中含有1molHe原子,含有的最外层电子的物质的量为2mol,含有最外层电子数为2NA,故A错误;
B.3.9g 2H37Cl的物质的量为0.1mol,0.1mol2H37Cl中含有2.1mol中子,含有的中子数为2.1NA,故B正确;
C.标准状况下11.2L丙烷的物质的量为0.5mol,0.5mol丙烷分子中含有1molC-C非极性键,含有的非极性键数目为NA,故C正确;
D.100mL 1mol•L-1 CH3COOH溶液中含有0.1mol醋酸,由于溶液中含有水分子,则该溶液含有的分子数目大于0.1NA,故D正确;
故选A.
点评 本题考查阿伏加德罗常数的计算与判断,题目难度中等,注意掌握以物质的量为中心的各化学量与阿伏加德罗常数的关系,试题有利于提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
9.化学与生活密切相关,下列说法错误的是( )
| A. | 食盐中加有碘,用其配成的溶液遇淀粉变蓝 | |
| B. | 厕所清洁剂、食用醋、肥皂水、厨房清洁剂四种溶液的pH逐渐增大 | |
| C. | 使用氯气自来水消毒时,氯气会与自来水中的有机物反应,生成的有机氯化物可能对人有害 | |
| D. | 硅胶、生石灰、氯化钙等都是食品包装袋中常用的干燥剂. |
7.Y元素的阳离子和X元素的阴离子具有与氩原子相同的电子层结构,下列叙述正确的是( )
| A. | Y的原子序数比X的大 | B. | Y的离子半径比X的离子大 | ||
| C. | Y原子的最外层电子数比X的大 | D. | Y元素的最高正价比X的大 |
14.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 在100 g质量分数为30%的甲醛水溶液中,含有氢原子数为2NA | |
| B. | 7.8 g Na2S和Na2O2固体混合物中,含有的阴离子数为0.1NA | |
| C. | 1mol乙醇含有共价键的总数7NA | |
| D. | 反应2SO2(g)+O2(g)?2 SO3 (g),单位时间内消耗NA个O2分子的同时生成2NA个SO3分子,此时反应达到平衡状态 |
4.如图所示,△E1=393.5kJ,△E2=395.4kJ,下列说法正确的是( )
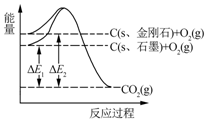

| A. | 1 mol石墨完全转化为金刚石需吸收1.9 kJ热量 | |
| B. | 石墨和金刚石的转化是物理变化 | |
| C. | 金刚石的稳定性强于石墨 | |
| D. | 1 mol金刚石和1 mol O2化学键断裂吸收的能量总和大于1 mol CO2分子中化学键断裂吸收的能量 |
8.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,11g CO2含有的共用电子对数为0.5NA | |
| B. | 1mol Na分别与足量的O2反应生成Na2O或Na2O2,失去的电子数均为NA | |
| C. | 通常状况下,39 g Na2O2固体中含有的离子总数为2NA | |
| D. | 滴加到沸水中的FeCl3溶液有5.6 g Fe3+发生水解,则生成的胶粒数为0.1NA |
9.某有机物Z具有较广泛的抗菌作用,其生成机理可由X与Y相互作用.下列有关叙述中不正确的是( )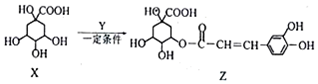

| A. | X能使酸性高锰酸钾溶液褪色 | |
| B. | Y的分子式为C9H8O3 | |
| C. | 1mol Z与足量NaOH溶液反应,最多消耗8mol NaOH | |
| D. | Z与浓溴水既能发生取代反应又能发生加成反应 |