题目内容
某元素同位素的单质
Xc,极易形成
Xn-,下列说法不正确的是( )
b a |
b a |
| A、此气体分子中含有的中子数为b-a | ||
| B、此元素的离子中含有的电子数为a+n | ||
| C、此气体分子中含有的质子数为c(a+n) | ||
D、一个该同位素原子的质量约为
|
考点:质量数与质子数、中子数之间的相互关系
专题:原子组成与结构专题
分析:A、中子数=质量数-质子数;
B、阴离子的电子数=质子数+离子的电荷数;
C、分子的质子数等于各原子的质子数之和;
D、原子的质量为原子的相对原子质量和阿伏伽德罗常数的比值.
B、阴离子的电子数=质子数+离子的电荷数;
C、分子的质子数等于各原子的质子数之和;
D、原子的质量为原子的相对原子质量和阿伏伽德罗常数的比值.
解答:
解:A、某元素同位素的单质
Xc,原子的中子数=质量数-质子数=b-a,则分子的中子数为c(b-a),故A错误;
B、阴离子的电子数=质子数+离子的电荷数,则该元素的离子中含有的电子数为a+n,故B正确;
C、分子的质子数等于各原子的质子数之和,则此气体分子中含有的质子数为ca,故C错误;
D、原子的质量为原子的相对原子质量和阿伏伽德罗常数的比值,即
g,故D正确.
故选AC.
b a |
B、阴离子的电子数=质子数+离子的电荷数,则该元素的离子中含有的电子数为a+n,故B正确;
C、分子的质子数等于各原子的质子数之和,则此气体分子中含有的质子数为ca,故C错误;
D、原子的质量为原子的相对原子质量和阿伏伽德罗常数的比值,即
| b |
| 6.02×1023 |
故选AC.
点评:本题考查了质子数、质量数和中子数之间的关系,题目难度不大,明确阴阳离子核外电子数的计算方法.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
下列离子方程式书写正确的是( )
| A、Ca(HCO3)2溶液中滴入过量 NaOH 溶液:HCO3-+Ca2++OH-═CaCO3↓+H2O |
| B、向NaAlO2 溶液中通人过量的 C02:CO2+2H20+A102-═Al(OH)3↓+HCO3- |
| C、0.01mol/L NH4Al(SO4)2 溶液与 O.02mol/L Ba(OH)2溶液等体积混合:Al3++2S042-+2Ba2++40H-═2BaSO4↓+AlO2-+2H20 |
| D、向Ca(ClO)2溶液中通入过量的 SO2:C10-+SO2+H2O═HClO+HSO3- |
用石墨电极电解CuSO4和KNO3的混合溶液500mL,经一段时间电解后,两极都得到11.2L气体(标准状况),此混合液中Cu2+的物质的量浓度为( )
| A、0.5mol/L |
| B、0.8mol/L |
| C、1mol/L |
| D、1.5mol/L |
下列分子中指定的碳原子(用*标记)不属于手性碳原子的是( )
A、苹果酸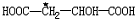 |
B、丙氨酸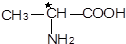 |
C、葡萄糖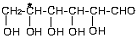 |
D、甘油醛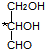 |
用铂作电极电解一定浓度的下列物质的水溶液.电解结束后,向剩余电解液中加适量水,能使溶液和电解前相同的是( )
| A、AgNO3 |
| B、HCl |
| C、NaOH |
| D、NaCl |
有两种气态烃的混合物,将该混合物2.24L(标准状况)完全燃烧,产物先后通过盛浓硫酸洗气瓶和碱石灰的干燥管(假设吸收完全),洗气瓶和干燥管的质量分别增加4.5g和13.2g.则该混合气体的组成和比例可能是( )
| A、CH4和C4H6 1:1 |
| B、CH4和C4H10 5:1 |
| C、C3H4和C3H8 3:1 |
| D、C2H2和C4H8 任意比 |
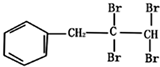 与NaOH的水溶液共热的化学方程式为
与NaOH的水溶液共热的化学方程式为
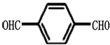 )的氧化产物“对苯二甲酸”与“乙二醇”发生缩聚,生成的聚酯纤维(涤纶)的结构简式为
)的氧化产物“对苯二甲酸”与“乙二醇”发生缩聚,生成的聚酯纤维(涤纶)的结构简式为