题目内容
W、X、Y、Z是核外电子层数相同且原子序数依次增大的短周期元素,W、X是金属元素,Y的氢化物为H2Y,Z的某种含氧酸有漂白性。W、X的最高价氧化物对应的水化物可以发生反应生成盐和水。下列判断正确的是
A.X的金属性强于W的金属性
B.W、X分别与Z形成的化合物都是离子化合物
C.W、X、Y、Z的简单离子的半径:Y>Z>W>X
D.Y的氧化物通入含有Z单质的溶液中,一定无明显变化
C
【解析】
试题分析:根据题意知,W、X、Y、Z是核外电子层数相同且原子序数依次增大的短周期元素,则4种元素同周期,Z的某种含氧酸有漂白性,则Z是氯元素;Y的氢化物为H2Y,则Y为硫元素;W、X是金属元素,W、X的最高价氧化物对应的水化物可以发生反应生成盐和水,则W是Na元素,X是Al元素。A.W是Na元素,X是Al元素,铝的金属性弱于钠的金属性,错误;B、氯化钠为离子化合物,而AlCl3是共价化合物,错误;C、根据离子半径比较原则判断,Na、Al、S、Cl的简单离子的半径:S2—>Cl—>Na+> Al 3+,即 Y>Z>W>X,正确;D、Y的氧化物二氧化硫通入含有氯单质的溶液中,二者反应生成硫酸和盐酸,氯水的浅绿色褪去,错误。
考点:考查元素推断、元素周期律。

练习册系列答案
相关题目
 Fe(SCN)2+(aq) 已知某一条件下,反应达到平衡时,Fe(SCN)2+的物质的量浓度与温度的关系如图所示,下列说法正确的是
Fe(SCN)2+(aq) 已知某一条件下,反应达到平衡时,Fe(SCN)2+的物质的量浓度与温度的关系如图所示,下列说法正确的是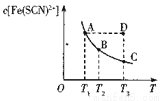

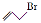 。则有机物
。则有机物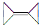 的二氯代物有
的二氯代物有 )的废水可以通过构成微生物电池除去,其原理如下图所示。
)的废水可以通过构成微生物电池除去,其原理如下图所示。
