题目内容
常温下0.1mol?L-1氨水的pH=a,下列能使溶液pH=(a+1)的措施是( )
| A、加入适量的氢氧化钠固体 |
| B、将溶液稀释到原体积的10倍 |
| C、加入等体积0.2mol?L-1氨水 |
| D、降低溶液的温度 |
考点:弱电解质在水溶液中的电离平衡,pH的简单计算
专题:电离平衡与溶液的pH专题
分析:一水合氨是弱电解质,所以氨水中存在电离平衡,氨水溶液的pH增大1,则溶液c(OH-)增大,可促进一水合氨的电离或加入碱,以此解答该题.
解答:
解:A.0.1mol/L氨水中加入NaOH固体,溶液中OH-的浓度增大,可知pH增大1,故A正确;
B.将溶液稀释到原体积的10倍,溶液c(OH-)减小,pH减小,故B错误;
C.加入等体积0.2mol?L-1氨水,混合后氨水浓度为0.15mol?L-1,c(OH-)不可能为混合前的10倍,故C错误;
D.降低溶液的温度,抑制一水合氨的电离,溶液pH减小,故D错误.
故选A.
B.将溶液稀释到原体积的10倍,溶液c(OH-)减小,pH减小,故B错误;
C.加入等体积0.2mol?L-1氨水,混合后氨水浓度为0.15mol?L-1,c(OH-)不可能为混合前的10倍,故C错误;
D.降低溶液的温度,抑制一水合氨的电离,溶液pH减小,故D错误.
故选A.
点评:本题考查弱电解质的电离,为高频考点和常见题型,侧重于学生的分析能力的考查,注意把握影响因素和pH的相关计算,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
某无色溶液中含有大量KOH,Na2CO3,Na2SO4,为验证其中阴离子,若限定只能使用试管和胶头滴管且只准取一次待测液,则加入试剂顺序正确的是( )
| A、BaCl2溶液,盐酸,酚酞 |
| B、BaCl2溶液,酚酞,盐酸 |
| C、酚酞,BaCl2溶液,盐酸 |
| D、酚酞,盐酸,BaCl2溶液 |
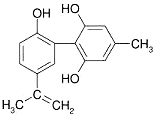 “人文奥运”的一个重要体现是坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如下图所示,有关该物质的说法正确的是( )
“人文奥运”的一个重要体现是坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如下图所示,有关该物质的说法正确的是( )| A、该分子中的碳原子均为不饱和碳原子 |
| B、滴入酸性KMnO4溶液,观察紫色褪去,能证明结构中存在碳碳双键 |
| C、1mol该物质分别与浓溴水和H2反应,最多消耗Br2和H2的物质的量分别为4mol、7mol |
| D、遇FeCl3溶液呈紫色,因为该物质与苯酚属于同系物 |
鉴别苯酚、苯、环己烯、四氯化碳、乙醇、碘化钠溶液,应选用的一种试剂是( )
| A、稀盐酸 |
| B、FeCl3溶液 |
| C、浓溴水 |
| D、酸性高锰酸钾溶液 |
四种元素的离子:aXm+、bYn+、cZn-、dRm-(a、b、c、d为元素的原子序数),它们具有相同的电子层结构,若m>n,对下列叙述的判断正确的是( )
| A、元素的原子序数:a>b>c>d |
| B、a-b=n-m |
| C、元素的非金属性:R>Z |
| D、最高价氧化物对应的水化物的碱性:X>Y |
等物质的量浓度的下列五种溶液,①CH3COOH ②(NH4)2CO3③NaHSO4④NaHCO3⑤Ba(OH)2,溶液中水的电离程度由大到小排列正确的是( )
| A、⑤③①④② |
| B、③⑤①②④ |
| C、②④③①⑤ |
| D、②④①③⑤ |
 A、B、C、D、E是中学常见的单质,X是化合物.A、B均为常见的金属,且在地壳中的含量分别为金属元素的前两位;常温下C是气态非金属单质,可以燃烧;D是空气主要成份之一,可与C发生重要工业反应生成X;E是固体非金属单质,在氧气中燃烧时有明亮的蓝紫色火焰.根据上述物质的信息,回答下列有关问题:
A、B、C、D、E是中学常见的单质,X是化合物.A、B均为常见的金属,且在地壳中的含量分别为金属元素的前两位;常温下C是气态非金属单质,可以燃烧;D是空气主要成份之一,可与C发生重要工业反应生成X;E是固体非金属单质,在氧气中燃烧时有明亮的蓝紫色火焰.根据上述物质的信息,回答下列有关问题: