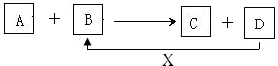
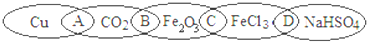题目内容
下列各组物质中所含原子数相同的是( )
| A、2 L CO和2 L O2 |
| B、同温同压下,2LO2和N2与NO的混合气体2L |
| C、0.2 mol H2和4.48 L HCl |
| D、标准状况下2 mol CO2和44.8 L水 |
考点:物质的量的相关计算
专题:计算题
分析:A.CO与氧气不一定处于相同的条件下,温度、压强会影响分子数目;
B.同温同压下,其体积之比等于其物质的量之比,均为双原子分子,含有原子数目相等;
C.HCl的不一定处于标况下;
D.标况下水不是气体.
B.同温同压下,其体积之比等于其物质的量之比,均为双原子分子,含有原子数目相等;
C.HCl的不一定处于标况下;
D.标况下水不是气体.
解答:
解:A.体积相等相等的条件下,温度、压强会影响分子数目,二者温度、压强不一定相同,二者含有原子数目不一定相等,故A错误;
B.同温同压下,2LO2和N2与NO的混合气体2L含有分子数目相等,均为双原子分子,含有原子数目相等,故B正确;
C.HCl的不一定处于标况下,4.48L HCl的物质的量不一定是0.2mol,与0.2 mol H2含有原子数目不一定相等,故C错误;
D.标况下水不是气体,44.8 L水的物质的量远远大于2mol,故D错误,
故选B.
B.同温同压下,2LO2和N2与NO的混合气体2L含有分子数目相等,均为双原子分子,含有原子数目相等,故B正确;
C.HCl的不一定处于标况下,4.48L HCl的物质的量不一定是0.2mol,与0.2 mol H2含有原子数目不一定相等,故C错误;
D.标况下水不是气体,44.8 L水的物质的量远远大于2mol,故D错误,
故选B.
点评:本题考查气体摩尔体积,难度不大,注意气体摩尔体积的使用条件与对象,注意根据PV=nRT理解温度、压强对气体摩尔体积的影响.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案
相关题目
化学式为C5H10的链状烃有(考虑顺反异构体)( )
| A、3种 | B、4种 | C、5种 | D、6种 |
H+(aq)+OH-(aq)=H2O(l)△H=a,则a可能等于( )
| A、-57.3mol/L |
| B、-57.3kJ/mol |
| C、+57.3J/mol |
| D、-57.3J/mol |
同温同压下,等质量的O2和CO2相比较,下列叙述正确的是( )
| A、体积比为8:11 |
| B、分子个数之比为11:12 |
| C、物质的量之比为8:11 |
| D、原子个数之比为11:12 |
如图两瓶体积相等的气体,在同温、同压时瓶内气体的关系一定正确的是( ) 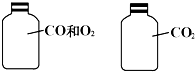
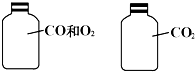
| A、所含原子数相等 |
| B、所含分子数相等 |
| C、气体质量相等 |
| D、所含C原子数相等 |
下列离子方程式书写正确的是( )
| A、稀硫酸跟铁反应:Fe+6H+=2Fe3++3H2↑ |
| B、稀硫酸与氢氧化钡溶液反应:H++OH-=H2O |
| C、碳酸钙放入稀盐酸中:CO32+2H+=CO2↑+H2O |
| D、稀盐酸放入碳酸钠中:CO32+2H+=CO2↑+H2O |
甲试管盛有Na2CO3和NaHCO3的混合溶液,乙试管盛有Na2SO3和NaHSO3的混合溶液,四种物质的浓度均为0.1mol?L-1,关于两混合溶液的比较,下列说法正确的是(已知:H2SO3的Ka1=1.3×10-2mol?L-1,Ka2=6.3×10-8mol?L-1;H2CO3的Ka1=4.2×10-7mol?L-1,Ka2=5.6×10-11mol?L-1)( )
| A、c(HCO3-)<c(CO32-) |
| B、两溶液都能使酸性高锰酸钾溶液褪色 |
| C、c(HCO3-)>c(HSO3-) |
| D、c(CO32-)+c(HCO3-)═c(SO32-)+c(HSO3-) |