题目内容
15.下列离子方程式正确的是( )| A. | 向盐酸中滴加氨水:H++OH-═H2O | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O | |
| C. | 铜溶于稀硝酸:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| D. | 向次氯酸钙溶液中通入过量CO2:Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO |
分析 A.一水合氨在离子反应中保留化学式;
B.发生氧化还原反应生成碘化亚铁、碘、水;
C.反应生成硝酸铜、NO和水;
D.反应生成碳酸氢钙、HClO.
解答 解:A.向盐酸中滴加氨水的离子反应为H++NH3.H2O═H2O+NH4+,故A错误;
B.Fe(OH)3溶于氢碘酸的离子反应为2Fe(OH)3+2I-+6H+═2Fe2++I2+6H2O,故B错误;
C.铜溶于稀硝酸的离子反应为3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,故C正确;
D.向次氯酸钙溶液中通入过量CO2的离子反应为ClO-+H2O+CO2═HCO3-+HClO,故D错误;
故选C.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.近年来科学家发现维生素C(C6H8O6)有防癌作用,下列关于维生素C的说法中不正确的是( )
| A. | 维生素C是有机物 | |
| B. | 一个维生素C分子中含有20个原子 | |
| C. | 一个维生素C分子由碳、氢、氧三种元素组成 | |
| D. | 某些蔬菜、水果中富含维生素C |
6.对于可逆反应N2(g)+3H2(g)?2NH3(g)△H<0,下列研究目的和图示相符的是( )
| 选项 | A | B |
| 研究目的 | 压强对反应的影响 | 温度对反应的影响 |
| 图示 |  |  |
| 选项 | C | D |
| 研究目的 | 平衡体系中增加N2对反应的影响 | 催化剂对反应的影响 |
| 图示 |  |  |
| A. | A | B. | B | C. | C | D. | D |
3.按要求回答下列问题
(1)写出下列物质在水中的电离方程式
①NaHCO3NaHCO3═Na++HCO3-;②HClOHClO?H++ClO-.
(2)若要除去下列溶液中的杂质(括号内为杂质),请将选用的试剂及有关反应的离子方程式填入下表的空白处:
(3)镁着火不能用二氧化碳来灭火,理由是2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C(用化学方程式表示)
(4)写出离子方程式CO32-+2H+═CO2↑+H2O所对应的化学方程式Na2CO3+2HCl=2NaCl+CO2+H2O.
(1)写出下列物质在水中的电离方程式
①NaHCO3NaHCO3═Na++HCO3-;②HClOHClO?H++ClO-.
(2)若要除去下列溶液中的杂质(括号内为杂质),请将选用的试剂及有关反应的离子方程式填入下表的空白处:
| 物质(杂质) | 试剂 | 有关离子方程式 |
| NaHCO3(Na2CO3) | ||
| FeCl2(FeCl3) |
(4)写出离子方程式CO32-+2H+═CO2↑+H2O所对应的化学方程式Na2CO3+2HCl=2NaCl+CO2+H2O.
10.蛇纹石矿可以看做是由MgO、Fe2O3、Al2O3、SiO2组成.由蛇纹石制取碱式碳酸镁的实验步骤如下:
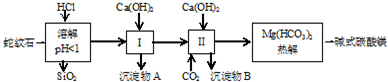
(1)蛇纹石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是Fe3+、Al3+.
(2)进行Ⅰ操作时,控制溶液pH=7~8(有关氢氧化物沉淀的pH见表)
Ca(OH)2不能过量,若Ca(OH)2过量可能会导致Al(OH)3溶解、Mg(OH)2沉淀生成.
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入过量NaOH(填入物质的化学式),然后过滤、洗涤、灼烧 (依次填写实验操作名称).
(4)Mg(HCO3)2热分解的反应方程式为:2 Mg(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$Mg2(OH)2CO3+3CO2↑+H2O.若热分解不完全,所得碱式碳酸镁中将混有MgCO3,则产品中镁的质量分数降低(填“升高”、“降低”或“不变”,已知碳酸镁的相对分子质量为84,碱式碳酸镁的相对分子质量为142).
(5)上述实验中,可以循环使用的物质是CO2(填写物质化学式).
(6)除去MgCl2酸性溶液中的Fe3+,可在加热、搅拌的条件下加入MgO或Mg(OH)2或MgCO3(试剂自选),过滤后再加入适量盐酸.

| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
(2)进行Ⅰ操作时,控制溶液pH=7~8(有关氢氧化物沉淀的pH见表)
Ca(OH)2不能过量,若Ca(OH)2过量可能会导致Al(OH)3溶解、Mg(OH)2沉淀生成.
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入过量NaOH(填入物质的化学式),然后过滤、洗涤、灼烧 (依次填写实验操作名称).
(4)Mg(HCO3)2热分解的反应方程式为:2 Mg(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$Mg2(OH)2CO3+3CO2↑+H2O.若热分解不完全,所得碱式碳酸镁中将混有MgCO3,则产品中镁的质量分数降低(填“升高”、“降低”或“不变”,已知碳酸镁的相对分子质量为84,碱式碳酸镁的相对分子质量为142).
(5)上述实验中,可以循环使用的物质是CO2(填写物质化学式).
(6)除去MgCl2酸性溶液中的Fe3+,可在加热、搅拌的条件下加入MgO或Mg(OH)2或MgCO3(试剂自选),过滤后再加入适量盐酸.
7.同温同压下,a g甲气体和2a g乙气体所占的体积之比为1:2,根据阿伏加德罗定律判断,下列叙述不正确的是( )
| A. | 同温同压下甲和乙的密度之比为1:1 | |
| B. | 等质量的甲和乙中的原子数之比为1:1 | |
| C. | 同温同体积下等质量的甲和乙的压强之比为1:1 | |
| D. | 甲与乙的相对分子质量之比为1:1 |
 工业尾气SO2有多种吸收和处理方法.
工业尾气SO2有多种吸收和处理方法.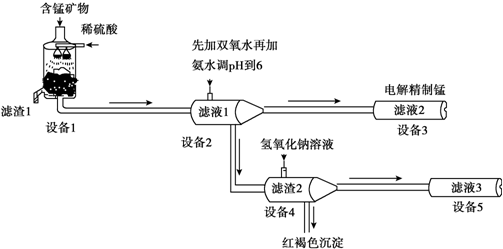
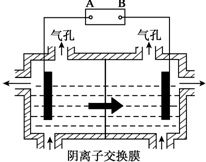 (5)设备3中用阴离子膜法提取金属锰的电解装置如图:
(5)设备3中用阴离子膜法提取金属锰的电解装置如图: