题目内容
下列电离或水解方程式中,正确的是
A.CH3COOH=CH3COO-+H+
B.Br-+H2O  HBr+OH-
HBr+OH-
C.CO32-+2H2O  H2CO3+2OH-
H2CO3+2OH-
D.NH4++2H2O
 NH3·H2O+H3O+
NH3·H2O+H3O+
【答案】
D
【解析】
试题分析:A、醋酸是弱电解质,存在电离平衡,电离方程式应该是CH3COOH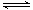 CH3COO-+H+,A不正确;B、氢溴酸是强酸,溴离子不水解,B不正确;C、碳酸是二元弱酸,CO32-水解分步进行,即CO32-+H2O
CH3COO-+H+,A不正确;B、氢溴酸是强酸,溴离子不水解,B不正确;C、碳酸是二元弱酸,CO32-水解分步进行,即CO32-+H2O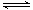 HCO3-+OH-、HCO3-+H2O
HCO3-+OH-、HCO3-+H2O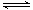 H2CO3+OH-,C不正确;D、氢离子在溶液中是以H3O+的形式存在的,因此NH4+的水解方程式也可以表示为NH4++2H2O
H2CO3+OH-,C不正确;D、氢离子在溶液中是以H3O+的形式存在的,因此NH4+的水解方程式也可以表示为NH4++2H2O  NH3·H2O+H3O+,D正确,答案选D。
NH3·H2O+H3O+,D正确,答案选D。
考点:考查水解方程式以及电离方程式的正误判断

练习册系列答案
相关题目



 2H++ SO3
2H++ SO3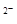
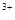 +3NH3·H2O=
Al(OH)3↓+3NH4+
+3NH3·H2O=
Al(OH)3↓+3NH4+