题目内容
19.硅橡胶具有无毒、无味、耐高温又耐低温,可制成耐温垫圈、密封件和人造心脏、人造血管等.它是由单体二甲基二氯硅烷(CH3)2SiCl2水解得到二甲基硅二醇,经脱水缩聚成的聚硅氧烷再经交联制成的.请用化学方程式写出上述二甲基二氯硅烷水解及线型缩聚的过程.分析 二甲基二氯硅烷[(CH3)2SiCl2]水解得到(CH3)2Si(OH)2和HCl,(CH3)2Si(OH)2发生缩聚反应生成聚硅氧烷,根据反应物和生成物书写方程式.
解答 解:二甲基二氯硅烷[(CH3)2SiCl2]水解得到(CH3)2Si(OH)2和HCl,反应方程式为:(CH3)2SiCl2+2H2O→(CH3)2Si(OH)2+2HCl;
(CH3)2Si(OH)2发生缩聚反应生成聚硅氧烷,反应方程式为n $\stackrel{一定条件下}{→}$(n-1)H2O+
$\stackrel{一定条件下}{→}$(n-1)H2O+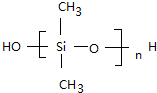 ,
,
答:其水解方程式为(CH3)2SiCl2+2H2O-→(CH3)2Si(OH)2+2HCl;缩聚反应方程式为n $\stackrel{一定条件下}{→}$(n-1)H2O+
$\stackrel{一定条件下}{→}$(n-1)H2O+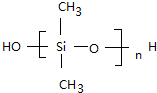 .
.
点评 本题考查化学方程式的书写,为高频考点,涉及缩聚反应、水解反应方程式的书写,明确断键和成键方式是解本题关键,题目难度不大.

练习册系列答案
相关题目
7.化学与社会、生活密切相关,下列说法中正确的是( )
| A. | “歼-20”飞机上使用的碳纤维是一种新型的有机高分子材料 | |
| B. | 高纯度的硅单质广泛用于制作光导纤维 | |
| C. | 汽车的排气管上装有“催化转化器”,使有毒的CO和NO反应生成N2和CO2 | |
| D. | Fe3O4俗称铁红,常作红色油漆和涂料 |
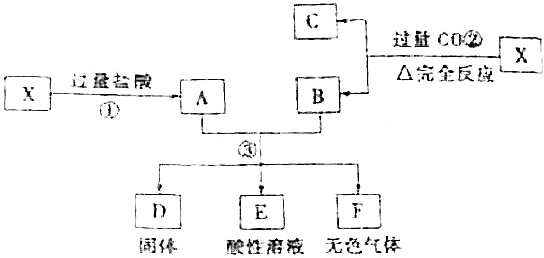
4.已知:CO2+NaOH(少量)=NaHCO3,CO2+2Na0H(过量)=Na2CO3+H2O,现用含0.2molNaOH的溶液吸收一定量的CO2,将所得熔液低温蒸干得到固体甲(该温度下NaHCO3不分解).下列说法正确的是( )
| A. | 固体甲一定是Na2CO3 | |
| B. | 固体甲一定是NaHCO3 | |
| C. | 当吸收0.15molCO2时,所得固体甲中Na2CO3和NaHCO3物质的量相等 | |
| D. | 在固体甲中加入足量稀盐酸,充分反应后蒸干所得溶液,得到11.7gNaCl |
11.若将浓硫酸慢慢滴入浓盐酸中,可能产生的实验现象是( )
| A. | 冒白雾,混合物温度升高 | B. | 产生黄绿色气体 | ||
| C. | 冒白雾,混合物温度降低 | D. | 液体四溅,冒白烟 |
9.关于卤素的下列叙述中正确的是( )
| A. | 卤素是典型的非金属元素,不能与其他非金属元素化合 | |
| B. | 卤素单质越活泼,其溶沸点就越低 | |
| C. | 卤素各单质都能和水剧烈反应 | |
| D. | 卤素气态氢化物的稳定性越强,还原性也越强 |
 .
.
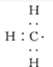 ;
;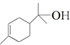 )的官能团的名称为碳碳双键、羟基;
)的官能团的名称为碳碳双键、羟基; 与溴发生加成反应的产物最多有4种,它们的结构简式为
与溴发生加成反应的产物最多有4种,它们的结构简式为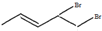 、
、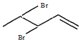 、
、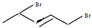 和
和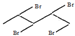 .
.