题目内容
2.硫及其化合物在国民生产中占有重要的地位.(1)常温常压下,已知1g 硫完全燃烧放出a kJ的热量,写出硫燃烧热的热化学方程式S(s)+O2(g)═SO2(g)△H=-32akJ/mol.
(2)又已知2H2S(g)+O2(g)═2S(s)+2H2O(l)△H=-bkJ/mol,写出H2S完全燃烧生成二氧化硫和水的热化学方程式2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H=-(b+64a) kJ/mol.
分析 (1)热化学方程式的书写,需要注意的有:物质的状态、反应热的数值与单位,反应热的数值与化学方程式前面的系数成正比;
(2)据S燃烧和氯化氢燃烧的热化学方程式,结合盖斯定律书写.
解答 解:(1)1g硫粉完全燃烧生成二氧化硫气体,放出a kJ的热量,所以32g硫粉完全燃烧生成二氧化硫气体,放出32akJ的热量,则热化学方程式为:S(s)+O2(g)═SO2(g)△H=-32akJ/mol,
故答案为:S(s)+O2(g)═SO2(g)△H=-32akJ/mol;
(2)已知①S(s)+O2(g)=SO2(g)△H=-32a kJ/mol②2H2S(g)+O2(g)=2S(s)+2H2O(l)△H=-bKJ•mol-1,据盖斯定律①×2+②得:2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H=-(b+64a) kJ/mol,
故答案为:2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H=-(b+64a) kJ/mol.
点评 本题考查了燃烧热的概念、热化学方程式的书写和盖斯定律、平衡常数的相关知识,题目难度不大.

练习册系列答案
 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案
相关题目
18.工业上可通过反应2Al2O3+3C+6Cl2$\frac{\underline{\;高温\;}}{\;}$AlCl3+3CO2制取无水氯化铝,下列有关该反应的说法正确的是( )
| A. | Cl2是氧化剂 | B. | Al2O3是还原剂 | C. | C发生还原反应 | D. | 氧原子得到电子 |
19.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | pH=1的溶液中:Fe2+、NO3-、Cl-、Na+ | |
| B. | 水电离出的c(H+)=10-12mol•L-1的溶液中:Ca2+、K+、Cl-、HCO3- | |
| C. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的水溶液中:NH4+、Al3+、NO3-、Cl- | |
| D. | 中性溶液中:Na+、Cl-、Fe3+、SO42- |
17.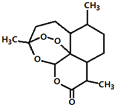 我国科学家屠呦呦获2015年诺贝尔生理学或医学奖.她研究得到的青蒿素挽救了数百万疟疾病人的生命,有关青蒿素说法不合理的是( )
我国科学家屠呦呦获2015年诺贝尔生理学或医学奖.她研究得到的青蒿素挽救了数百万疟疾病人的生命,有关青蒿素说法不合理的是( )
 我国科学家屠呦呦获2015年诺贝尔生理学或医学奖.她研究得到的青蒿素挽救了数百万疟疾病人的生命,有关青蒿素说法不合理的是( )
我国科学家屠呦呦获2015年诺贝尔生理学或医学奖.她研究得到的青蒿素挽救了数百万疟疾病人的生命,有关青蒿素说法不合理的是( )| A. | 化学式为C15H22O5 | |
| B. | 能发生取代反应和氧化反应 | |
| C. | 在H2SO4或 NaOH溶液中均不能稳定存在 | |
| D. | 可用乙醇从青蒿浸取液中萃取出青蒿素 |
7.已知甲醇的燃烧热数值为726.51kJ•mol-1.下列热化学方程式书写正确的是( )
| A. | CH4O+$\frac{3}{2}$O2═CO2+2H2O△H=-726.51 kJ•mol-1 | |
| B. | CH4O(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(g)△H=+726.51 kJ•mol-1 | |
| C. | 2CH4O(l)+3O2(g)═2CO2(g)+4H2O(l)△H=+1453.12 kJ•mol-1 | |
| D. | CH4O(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=-726.51 kJ•mol-1 |
14.下列物质的变化,不能通过一步化学反应完成的是( )
| A. | N2→NH3 | B. | SiO2→Na2SiO3 | C. | Na2O2→Na2CO3 | D. | SiO2→H2SiO3 |
11.下列关于钠的说法中不正确的是( )
| A. | 金属钠和氧气反应,条件不同,产物则不同 | |
| B. | 将钠投入氯化铵溶液中会有无色有刺激性气味的气体生成 | |
| C. | 当钠与硫酸铜溶液反应时,有大量红色固体铜生成 | |
| D. | 钠的化学性质比较活泼,少量的钠可以保存煤油中 |
12.光纤通信是以光作为信息的载体,让光在光导纤维中传播,制造光导纤维的原料是( )
| A. | 银 | B. | 铜 | C. | 铝 | D. | 石英砂 |