题目内容
15.工业上由钛铁矿(主要成分FeTiO3,含Fe2O3、A12O3、FeO、SiO2等杂质)制备TiCl4的工艺流程如图: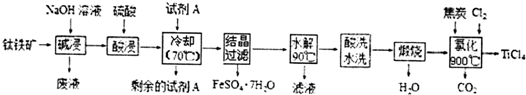
已知:①酸浸 FeTiO3(s)+2H2SO4(aq)═FeSO4(aq)+TiOSO4(sq)+2H2O(l)
②水解 TiOSO4(aq)+2H2O(l)$\frac{\underline{\;90℃\;}}{\;}$H2TiO3(s)+H2SO4(aq)
③煅烧 H2TiO3(s)$\frac{\underline{\;煅烧\;}}{\;}$TiO2(s)+H2O(g)
(1)FeTiO3中钛元素的化合价为+4,试剂A为Fe.
(2)碱浸过程发生的离子反应方程式为Al2O3+2OH-═2AlO2-+H2O;SiO2+2OH-═SiO32-+H2O.
(3)酸浸后需将溶液温度冷却至70℃左右,若温度过高会导致最终产品收率过低,原因是温度过高水导致TiOSO4提前水解生成H2TiO3沉淀.
(4)上述流程中氯化过程的化学反应方程式为TiO2+C+2Cl2$\frac{\underline{\;900℃\;}}{\;}$ TiCl4 +CO2.
已知TiO2(s)+2Cl2(g)?TiCl4(1)+O2(g)△H=+15l kJ•mol-1.该反应极难进行,当向反应体系中加入碳后,则反应在高温条件下能顺利发生.从化学平衡的角度解释原因是C与氧气反应减小氧气浓度,使平衡正向移动,C与氧气反应为放热反应,温度升高,使平衡正向移动,促使反应顺利进行.
(5)TiCl4极易水解,利用此性质可制备纳米级TiO2•xH2O,该反应的化学方程式是TiCl4+(x+2)H2O=TiO2•xH2O+4HCl.
分析 钛铁矿用氢氧化钠溶液溶解,氧化铝、二氧化硅反应溶解,过滤得到钛铁矿精矿中主要含有FeTiO3、Fe2O3、FeO,再用浓硫酸处理,得到强酸性溶液中含有TiOSO4、Fe2(SO4)3、FeSO4及未反应的硫酸等,加入试剂A后冷却、结晶、过滤得到硫酸亚铁晶体,则A为Fe,将Fe3+转化为Fe2+.滤液进行水解得到H2TiO3,用硫酸洗去杂化,再煅烧得到TiO2,TiO2、C、Cl2反应得到TiCl4及CO2.
(1)反应①为非氧化还原反应,结合化合价代数和为0计算;
(2)氧化铝与氢氧化钠反应生成偏铝酸钠与水,二氧化硅与氢氧化钠反应生成硅酸钠与水;
(3)温度过高水导致TiO2+水解;
(4)氯化过程是TiO2、C、Cl2反应得到TiCl4及CO2;
C与氧气反应降低氧气浓度,C与氧气反应为放热反应,有利于平衡正向移动;
(5)TiCl4极易水解得到TiO2•xH2O,还生成HCl.
解答 解:钛铁矿用氢氧化钠溶液溶解,氧化铝、二氧化硅反应溶解,过滤得到钛铁矿精矿中主要含有FeTiO3、Fe2O3、FeO,再用浓硫酸处理,得到强酸性溶液中含有TiOSO4、Fe2(SO4)3、FeSO4及未反应的硫酸等,加入试剂A后冷却、结晶、过滤得到硫酸亚铁晶体,则A为Fe,将Fe3+转化为Fe2+.滤液进行水解得到H2TiO3,用硫酸洗去杂化,再煅烧得到TiO2,TiO2、C、Cl2反应得到TiCl4及CO2.
(1)反应①为非氧化还原反应,结合化合价代数和为0,可知FeTiO3中钛元素的化合价为+4,由上述分析可知A为Fe,
故答案为:+4;Fe;
(2)氧化铝与氢氧化钠反应生成偏铝酸钠与水,二氧化硅与氢氧化钠反应生成硅酸钠与水,相应反应离子方程式为:Al2O3+2OH-═2AlO2-+H2O、SiO2+2OH-═SiO32-+H2O,
故答案为:Al2O3+2OH-═2AlO2-+H2O;SiO2+2OH-═SiO32-+H2O;
(3)温度过高水导致TiOSO4提前水解生成H2TiO3沉淀,Ti元素利用率减小,
故答案为:温度过高水导致TiOSO4提前水解生成H2TiO3沉淀;
(4)氯化过程是TiO2、C、Cl2反应得到TiCl4及CO2,反应方程式为:TiO2+C+2Cl2$\frac{\underline{\;900℃\;}}{\;}$ TiCl4 +CO2,
C与氧气反应减小氧气浓度,使平衡正向移动,C与氧气反应为放热反应,温度升高,使平衡正向移动,促使反应顺利进行,
故答案为:TiO2+C+2Cl2$\frac{\underline{\;900℃\;}}{\;}$ TiCl4 +CO2;C与氧气反应减小氧气浓度,使平衡正向移动,C与氧气反应为放热反应,温度升高,使平衡正向移动,促使反应顺利进行;
(5)TiCl4极易水解得到TiO2•xH2O,还生成HCl,反应方程式为:TiCl4+(x+2)H2O=TiO2•xH2O+4HCl,
故答案为:TiCl4+(x+2)H2O=TiO2•xH2O+4HCl.
点评 本题综合考查物质制备实验,关键是对工艺流程原理的理解,注意分析工艺流程中试剂线、原理线、操作线,要求学生具有一定分析和解决问题的能力,题目难度中等.

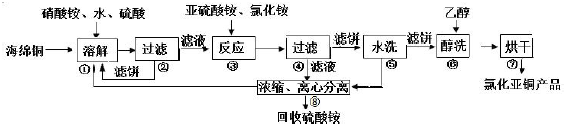
常见高铁酸钾的制备方法如下:
| 制备方法 | 具体内容 |
| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸钾和KNO2等产物 |
| 湿法 | 强碱性介质中,Fe(NO3)3与KClO反应生成紫红色高铁酸钾溶液 |
| 电解法 | 电解浓NaOH溶液制备Na2FeO4 |
(2)某湿法制备高铁酸钾的基本流程及步骤如下:
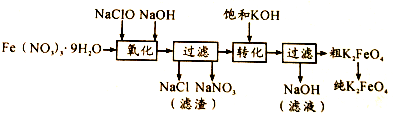
①控制反应温度为25℃,搅拌1.5h,经氧化等过程溶液变为紫红色,该反应的离子方程式为3ClO-+2Fe3++10OH-═2FeO42-+3Cl-+5H2O.
②在紫红色溶液中加入饱和KOH溶液,析出紫黑色晶体,过滤,得到K2FeO4粗产品.沉淀过程中加入饱和KOH溶液得到晶体的原因是该温度下高铁酸钾的溶解度比高铁酸钠的溶解度小.
③K2FeO4粗产品含有Fe(OH)3、KCl等杂质,用重结晶方法进行分离提纯.其提纯步骤为:将一定量的K2FeO4粗产品溶于冷的3mol/LKOH溶液中,过滤,将滤液置于冰水浴中,向滤液中加入饱和KOH溶液,搅拌、静置、过滤,用乙醇洗涤2~3次,在真空干燥箱中干燥.
④若以FeCl3 代替Fe(NO3)3作铁源,K2FeO4的产率和纯度都会降低.一个原因是在反应温度和强碱环境下NaCl的溶解度比NaNO3大,使得NaCl结晶去除率较低;另一个原因是Cl-被FeO42-氧化,消耗产品使产率降低.
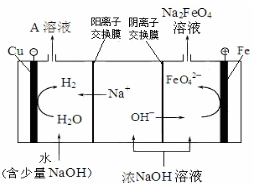
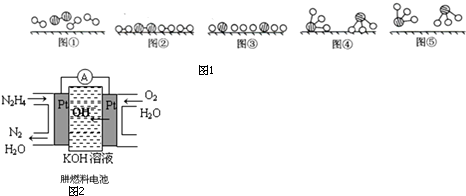
(3)工业上还可用通过电解浓NaOH溶液制备Na2FeO4,其工作原理如下图所示:阳极的电极反应为Fe-6e-+8OH-=FeO42-+4H2O;其中可循环使用的物质的电子式是
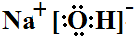 .
.
(4)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38、Ksp[Cu(OH)2]=2.2×10-20,向该温度下含有Fe3+、Cu2+浓度均为0.01mol/L的溶液中,滴加浓NaOH溶液,当溶液pH=10时,溶液中c(Cu2+):c(Fe3+)=5.5×1013:1.
| A. | 物质的量浓度相等的①NH4Cl ②(NH4)2SO4 ③NH4Al(SO4)2三种溶液中,c(NH4+由大到小的顺序为:③>②>① | |
| B. | 0.1mol•L-1CH3COOH与0.05mol•L-1NaOH溶液等体积混合(pH<7): c(CH3COO-)>c(Na+)>cCH3COOH)>c(H+) | |
| C. | 0.1 mol•L-1Na2CO3与0.05mol•L-1 NaHCO3溶液等体积混合: $\frac{3}{5}$c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| D. | 在0.1 mol•L-1NaHC2O4溶液(pH<7)中:c(OH-)+2c(C2O42-)=c(H+)+2c(H2C2O4) |
| 实验 编号 | 实验目的 | 温度/℃ | 催化剂 质量/g | 反应物初始浓度 /10-3mol•L-1 | |
| H2 | I2 | ||||
| Ⅰ | 为以下实验作参照 | 457 | 0 | 7 | 9 |
| Ⅱ | ① | 420 | ② | 7 | 9 |
| Ⅲ | 探究催化剂对该反应速率的影响 | ③ | 10 | 7 | 9 |
(2)实验Ⅰ中,I2的物质的量浓度(c)随时间(t)的变化如图所示.
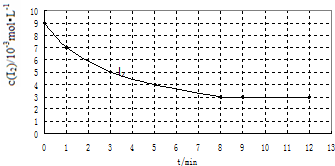
根据图中数据回答下列问题:
①在0~5min内反应的平均速率v(I2)=1×10-3mol•L-1•min-1.
②该温度下,反应的平衡常数K=$\frac{{c}^{2}(HI)}{c({H}_{2})×c({I}_{2})}$=48.(前空写表达式,后空写计算所得的数据)
③该同学还想用此反应研究压强对化学平衡移动的影响,请问能否达到实验目的?请说明原因.
不能(填“能”、不能”),原因是该反应前后气体计量数相等,平衡不受压强的影响.

 ,OPA分子中最多有16个原子共平面.
,OPA分子中最多有16个原子共平面.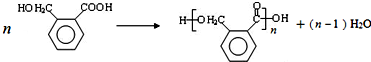 (不必注明反应条件),该反应的类型为缩聚反应.
(不必注明反应条件),该反应的类型为缩聚反应.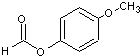 (写出其结构简式).
(写出其结构简式).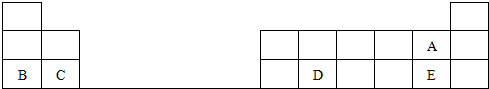
 .
.
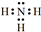 .
.
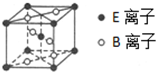 A、B、C、D、E为核电荷数依次增大的五种元素.A的基态原子中有2个未成对电子,B是地壳中含量最多的元素,C是短周期中最活泼的金属元素,D与C可形成CD型离子化合物,E的基态原子3d轨道上有2个电子.请回答下列问题:
A、B、C、D、E为核电荷数依次增大的五种元素.A的基态原子中有2个未成对电子,B是地壳中含量最多的元素,C是短周期中最活泼的金属元素,D与C可形成CD型离子化合物,E的基态原子3d轨道上有2个电子.请回答下列问题: