题目内容
下列叙述正确的是(用NA代表阿伏加德罗常数的值)( )
| A、2.4 g金属镁变为镁离子时失去的电子数为0.1NA |
| B、标准状况下,O2的体积约为22.4L |
| C、在标准状况下,22.4L CH4与18g H2O所含有电子数均为10NA |
| D、常温常压下,80g SO3含有的氧原子数无法计算 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.金属镁为2价金属,根据镁的物质的量计算出失去的电子数;
B.只知道标准状况,不知物质的量,无法计算氧气的体积;
C.根据每个CH4、H2O分子含有10个电子,在标准状况下,22.4L CH4与18g H2O的物质的量都是1mol计算;
D.根据质量和摩尔质量计算出物质的量,再计算出含有的氧原子数目.
B.只知道标准状况,不知物质的量,无法计算氧气的体积;
C.根据每个CH4、H2O分子含有10个电子,在标准状况下,22.4L CH4与18g H2O的物质的量都是1mol计算;
D.根据质量和摩尔质量计算出物质的量,再计算出含有的氧原子数目.
解答:
解:A.2.4g金属镁的物质的量为0.1mol,变为镁离子时失去0.2mol电子,失去的电子数为0.2NA,故A错误;
B.只知道标准状况,不知物质的量,无法计算氧气的体积,故B错误;
C.每个CH4、H2O分子含有10个电子,在标准状况下,22.4L CH4与18g H2O的物质的量都是1mol,所含有电子数均为10NA,故C正确;
D.常温常压下,80gSO3的物质的量为1mol,含有的氧原子数为3NA,故D错误;
故选C.
B.只知道标准状况,不知物质的量,无法计算氧气的体积,故B错误;
C.每个CH4、H2O分子含有10个电子,在标准状况下,22.4L CH4与18g H2O的物质的量都是1mol,所含有电子数均为10NA,故C正确;
D.常温常压下,80gSO3的物质的量为1mol,含有的氧原子数为3NA,故D错误;
故选C.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,它既考查了学生对物质的量、粒子数、质量、体积等与阿伏加德罗常数关系的理解,又可以涵盖多角度的化学知识内容.

练习册系列答案
相关题目
下列叙述错误的是( )
| A、点燃甲烷前不一定要事先验纯 |
| B、甲烷燃烧能放出大量的热,所以是一种气体燃料 |
| C、甲烷可用来制炭黑和氢气 |
| D、煤矿矿井要注意通风和严禁烟火,以免发生爆炸事故 |
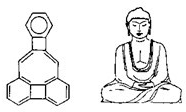 美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛(如图).因而称为释迦牟尼分子(所有原子在同一平面).有关该有机分子的说法不正确的是( )
美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛(如图).因而称为释迦牟尼分子(所有原子在同一平面).有关该有机分子的说法不正确的是( )| A、该有机物属于芳香烃 |
| B、该有机物属于苯的同系物 |
| C、该有机物分子中含有22个碳原子 |
| D、该有机物可发生加成反应 |
下列叙述中,正确的是( )
| A、一个基态多电子的原子中,可以有运动状态完全相同的电子 |
| B、元素原子的最外层电子数等于元素的最高正价 |
| C、凡是中心原子采取sp3杂化轨道成键的分子其立体构型都是正四面体 |
| D、电子构型为[Ar]3d54s2的元素是过渡元素 |
下列溶液一定呈中性的是( )
| A、将pH=5的盐酸稀释100倍所得溶液 |
| B、c(H+)=1.0×10-7mol/L |
| C、c(H+)=c(OH-)=1×10-6mol/L的溶液 |
| D、非电解质溶于水得到的溶液 |
下列各组溶液中离子,能在溶液中大量共存的是( )
| A、H+、Ca2+、NO3-、CO32- |
| B、K+、Na+、Cl-、NO3- |
| C、Ag+、Na+、Cl-、K+ |
| D、NH4+、K+、NO3-、SO42- |
在下列无色透明溶液中,能大量共存的离子组是( )
| A、Cu2+、Na+、SO42-、Cl- |
| B、Ca2+、HCO3-、Cl-、OH- |
| C、Ba2+、H+、I-、SO42- |
| D、Mg2+、Na+、NH4+、NO3- |
下列说法中正确的是( )
| A、熔化状态下能导电的物质一定是离子化合物 |
| B、离子化合物不可能只含非金属元素 |
| C、离子化合物均能溶于水 |
| D、离子化合物在一定条件下可以转化成分子 |